Application Note 拍動するAxiogenesis Cor.4UヒトiPS細胞由来心筋細胞における
カルシウムトランジェントへの化合物の影響
- 創薬初期段階における化合物の毒性と有効性の評価
- 生理学的関連性の高いシステムによる心毒性プロファイルの解析
- スループット要件に応じたアッセイ規模の調整
PDF版(英語)
はじめに
創薬プロセスの初期段階において心毒性を評価することは、潜在的に毒性を持つ化合物を早期に開発から除外するために重要です。これは、心毒性評価で失敗する化合物に起因する非効率性や高コストを削減するうえで極めて重要です。近年では、生物学的に関連性の高い細胞ベースモデルを用いた、予測精度の高いin vitro心毒性アッセイのニーズが高まっています。iPS細胞由来心筋細胞は、ネイティブな心筋細胞に類似した遺伝子発現プロファイルおよび表現型特性を示すことから、特に魅力的な細胞モデルです。化合物は心筋細胞におけるカルシウムシグナルのオシレーションに干渉する可能性があり、カルシウムシグナルのオシレーションは細胞質内カルシウム濃度の変化を反映しています。カルシウム感受性色素を用いることで、心筋細胞内のカルシウム濃度が筋小胞体からのCa²⁺放出により上昇する際に蛍光シグナルが増加し、細胞の収縮過程を示します。逆に、Ca²⁺が細胞質から筋小胞体へ能動的に輸送されることで濃度が低下し、細胞の弛緩過程を示す蛍光シグナルの減少が観察されます。
EarlyTox™ 心毒性キットに含まれるカルシウム感受性色素を用いることで、Axiogenesis Cor.4U® iPS細胞由来心筋細胞におけるカルシウムピーク頻度の濃度依存的な変調やオシレーションパターンの可視化が可能になります。FLIPR® TetraシステムまたはSpectraMax® i3 マルチモードマイクロプレートリーダーを用いて測定を行います。ピーク頻度、振幅、ピーク幅、立ち上がり時間、減衰時間などのパラメータの変化を解析することで、潜在的な毒性の予測や、前臨床開発やメディシナルケミストリーに進めるべきでない化合物の除外が可能になります。さらに、この手法は心筋細胞に治療効果をもたらす可能性のある化合物の探索や、新規心疾患治療薬のリード化合物の同定にも活用できます。
材料と方法
EarlyTox 心毒性キット(図1)を用いて、カルシウムオシレーションに影響を与える4種類の化合物の挙動を評価しました。拍動頻度およびオシレーションパターンは、心筋細胞に対する治療効果や心毒性の可能性を示す指標となります。
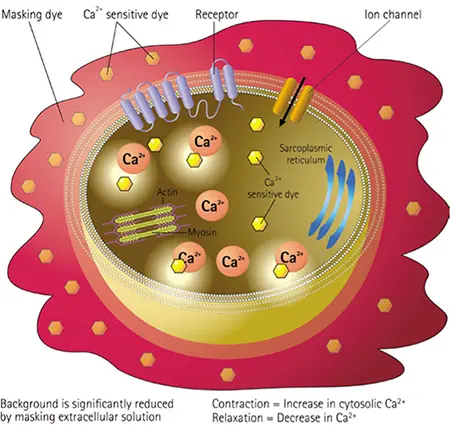
図1. EarlyTox 心毒性キットのアッセイ原理 本キットには、カルシウム感受性色素と、心筋細胞の拍動に伴う細胞質カルシウム濃度の変化を測定するために最適化された独自のマスキング色素が含まれています。iPS細胞由来心筋細胞や初代心筋細胞に対する薬理学的化合物の影響を評価するために使用できます。
このアッセイでは、Axiogenesis, AG, Cologne, Germanyから提供されたヒトCor.4U iPS細胞由来心筋細胞を、フィブロネクチンでコーティングされた黒壁の透明底384ウェルプレートに、1ウェル当たり11,000個の総細胞数でプレーティングしました。Cor.4Uプロトコールに従い、細胞を実験の3日前にプレーティングし、5% CO2、37℃でインキュベートしました。セルにはCor.4U培地を毎日与えました。
3日目には、細胞はシート状に広がり、ギャップ結合を形成し、同期して拍動を開始しました。アッセイの2時間前に新鮮な培地で給餌し、再度インキュベーターに戻しました。EarlyTox 心毒性キットの色素(モレキュラーデバイス #R8210)をCor.4U培地10 mLに希釈し、37°Cに加温して染色用バッファを調製しました。これは、色素添加による拍動の低下を防ぐためです。細胞25 μLに対して色素25 μLを加え、プレートを再び5% CO₂、37°Cのインキュベーターに2時間戻しました。
染色中に、DPBSバッファ中に心筋活性化合物を5倍濃度で調製した化合物プレートを作成しました。温度変化による細胞への影響を最小限に抑えるため、化合物プレートも37°Cに加温しました。FLIPR Tetraシステムで測定する場合は、検出中に各ウェルに12.5 μLの化合物をオンラインで添加し、SpectraMax i3リーダーで測定する場合は、検出の1時間前にオフラインで添加しました。FLIPR Tetraシステムでは、化合物添加後3分でデータを取得しました。パラメータの解析にはScreenWorks® Peak Proソフトウェアを使用し、信号トレースやカーブの描画にはGraphPad Prismを使用しました。
ScreenWorks PeakPro ソフトウェア
ScreenWorks Peak Proソフトウェアは、拍動細胞から得られるトランジェント信号の解析に使用されました。このモジュールは、ScreenWorksソフトウェアに追加されたもので、拍動細胞からのデータを迅速に解析することが可能です。解析可能なパラメータには、ピーク頻度、ピーク数、不規則な間隔などが含まれます。さらに、ピーク振幅、ピーク幅(50%および10%の高さ)、間隔、立ち上がり時間、減衰時間の平均値および標準偏差も取得可能です。
SpectraMax i3 マルチモードマイクロプレートリーダーでの心筋細胞アッセイ
SpectraMax i3プレートリーダーでのアッセイでは、化合物は測定の1時間前にオフラインで添加されました。SoftMax® Proソフトウェアを用いて、信号トレースの表示、パラメータの計算、カーブの描画を行いました。
結果
FLIPR Tetraシステムによる化合物の影響評価
EarlyTox 心毒性色素は、心筋細胞におけるカルシウムシグナルの変化を追跡します。拍動中の信号トレースでは、細胞質内Ca²⁺濃度が筋小胞体からの放出により上昇することで蛍光シグナルが増加し、収縮過程を示します。逆に、Ca²⁺が細胞質から筋小胞体へ能動的に輸送されることで濃度が低下し、弛緩過程を示す蛍光シグナルの減少が観察されます。図2には、FLIPR Tetraシステムで記録された、コントロールウェルにおける心筋細胞の拍動に伴う蛍光シグナルの変化例を示しています。
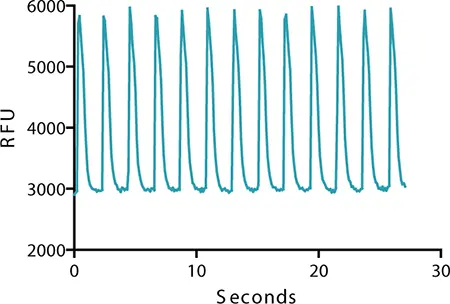
図2:カルシウムシグナルのオシレーション 実験コントロールでは、EarlyTox 心毒性キットを用いてFLIPR Tetraシステムで測定したCor.4U iPS細胞由来心筋細胞におけるカルシウムシグナルのオシレーションが、細胞質内カルシウム濃度の変化を反映しています。
心筋細胞にはβアドレナリン受容体(GPCR)が存在することが報告されています*1。作動薬および拮抗薬は、それぞれ拍動頻度やシグナル特性に正または負の影響を与える可能性があります。図3は、非選択的作動薬であるイソプロテレノールの例です。拍動パターンと拍動頻度の変化が示されています。ウェルあたりのイソプロテレノール濃度が増加するにつれて、化合物添加3分後の拍動数は28 BPMから50 BPMへと増加しました。一方、臨床的に不整脈患者に処方されるβアドレナリン拮抗薬プロプラノロールは、iPS細胞由来心筋細胞の拍動頻度を低下させました(図4)。さらに、カルシウムトランジェントシグナルの振幅も減少しました。
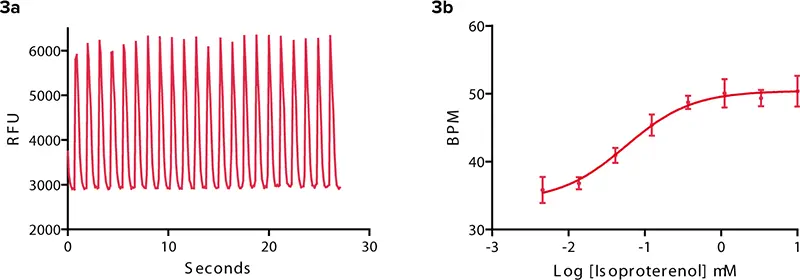
図3:イソプロテレノール(βアドレナリン作動薬)(3a) 0.37 μMイソプロテレノールに対するカルシウムシグナルのオシレーション。コントロールは図2に示されています。(3b) 化合物添加3分後、イソプロテレノール濃度の増加に伴い、拍動頻度は約36 BPMから50 BPMに上昇。
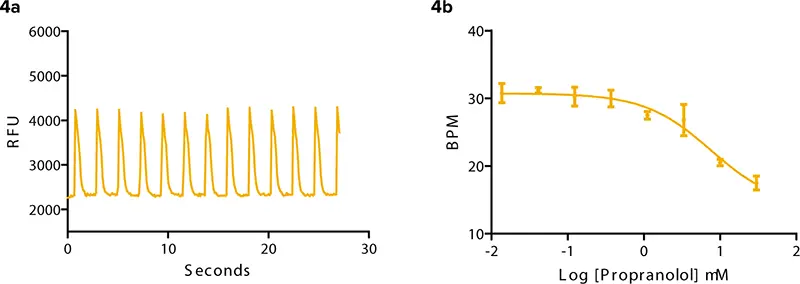
図4:プロプラノロール(βアドレナリン拮抗薬)(4a) 3.3 μMプロプラノロールに対する拍動パターン。(4b) 化合物添加3分後、濃度の増加に伴い拍動頻度は約31 BPMから17 BPMに低下。
シサプリドは、かつて胃食道逆流症の治療薬として使用されていましたが、心臓のhERGチャネルを阻害することが判明し、米国では市場から撤退しました。図5に示すように、シサプリドは明確に異なる拍動パターンを示し、図2のコントロールと比較して拍動頻度が著しく低下しました。さらに、ScreenWorks PeakProソフトウェアで算出された10%振幅におけるピーク幅(秒)は、シサプリド濃度の増加に伴い拡大しました。拍動するiPS細胞由来心筋細胞におけるカルシウムシグナルの変化を検出することは、安全性関連化合物の早期同定において重要な手法です。
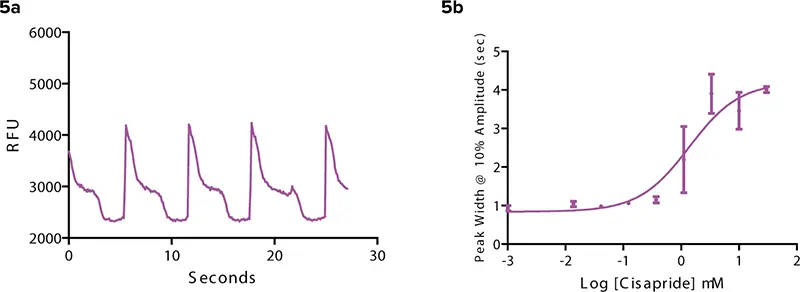
図5:シサプリド(hERG阻害薬)(5a) 図2のコントロールと比較して、シサプリドは明確に異なる拍動パターンを示す。(5b) 化合物添加3分後、シサプリド濃度の増加に伴い、10%振幅におけるピーク幅(秒)が増加。
PeakProソフトウェアによる解析では、シサプリド濃度の増加に伴い、ピーク幅(10%振幅)の値が増加しました。拍動するiPS細胞由来心筋細胞におけるカルシウムシグナルの変化を検出することは、安全性に関わる化合物を早期に同定するための重要な手段です。
SpectraMax i3 マルチモードマイクロプレートリーダーによる化合物の影響評価
別の実験では、Cor.4U iPS細胞由来心筋細胞に色素をロードし、リドカインを1時間処理しました。リドカインはナトリウムチャネル阻害薬であり、濃度の増加に伴い心筋細胞の拍動頻度を低下させます。カルシウムトランジェントシグナルはSpectraMax i3プレートリーダーで40秒間測定されました。各ウェルを個別に読み取ることで、細胞の拍動頻度(BPM)を評価しました(図6)。FLIPR Tetraシステムでのコントロール細胞と比較して、SpectraMax i3でのコントロール細胞の拍動はやや遅かったものの、リドカイン濃度の増加に伴うBPMの変化は明確に確認できました。
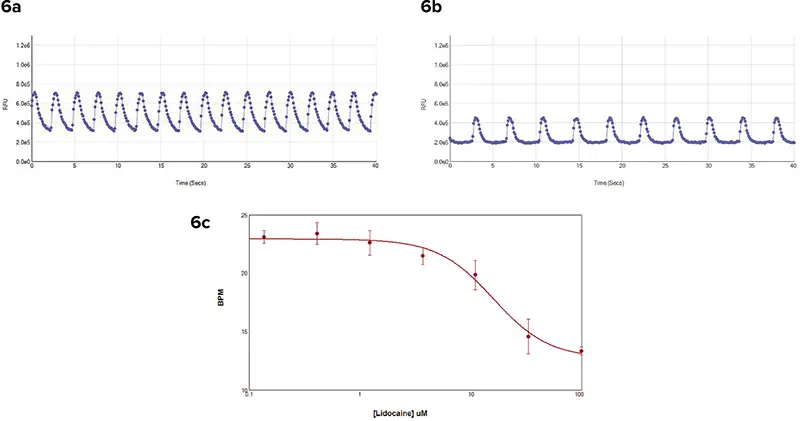
図6:Cor.4U iPS細胞由来心筋細胞のカルシウムトランジェントシグナル SpectraMax i3リーダーで測定。データ解析はSoftMax Proソフトウェアを使用。(6a) コントロール細胞の拍動パターン。(6b) 処理細胞の拍動パターン。(6c) 濃度反応曲線により、リドカイン処理1時間後の拍動頻度の低下を確認。
結論
EarlyTox 心毒性キットは、リード化合物の最適化段階において、化合物の毒性および有効性を迅速かつ簡便に予測できる信頼性の高いアッセイを提供します。Cor.4U iPS細胞由来心筋細胞とFLIPR TetraシステムまたはSpectraMax i3プレートリーダーを組み合わせることで、生理学的関連性の高い心毒性アッセイにおいて機能的プロファイルを評価し、色素による非特異的なカルシウムシグナルへの影響を最小限に抑えつつ、スループット要件に応じたアッセイのスケーリングが可能となります。
参考文献
- Jaffar, M., et al., The case for induced pluripotent stem cell-derived cardiomyocytes in pharmacological screening, British Journal of Pharmacology (2013) 169: 304-317.
PDF版(英語)