Application Note 血清中のSARS-CoV-2 IgGを
高感度発光アッセイで測定
- 均一な非洗浄型フォーマットでハイスループットスクリーニング(HTS)にスケールアップできます
- サンプル量はわずか15 μLで使用可能です
- 1時間以内に結果を取得できます
PDF版(英語)
はじめに
Joyce Itatani | Applications Scientist | モレキュラーデバイス
Cathy Olsen, PhD | Sr. Applications Scientist | モレキュラーデバイス
SARS-CoV-2に対する免疫応答の一環として、感染者は症状発現後1~3週間以内に血中で検出可能なウイルス特異的抗体を産生します。免疫グロブリンG(IgG)とIgMはほぼ同時に出現し、IgGはより長期間高レベルで維持されます *1,2。感染またはワクチン接種によって血清中に検出可能な抗体が存在することは、将来の感染に対する防御に寄与しますが、これらの抗体が持続する期間や防御の程度は、SARS-CoV-2に関する多くの未解明な課題の一部であり、現在も集中的に研究されています。
ヒト血清中のSARS-CoV-2抗体を検出するためのイムノアッセイは、この疾患の理解を深めるだけでなく、ワクチン研究においても重要なツールです。Promega Lumit™ Dx SARS-CoV-2イムノアッセイは、SARS-CoV-2スパイクタンパク質の受容体結合ドメイン(RBD)の断片を使用し、SmBiTとLgBiTというNanoLuc®ルシフェラーゼの2つのサブユニットで標識します。これらのサブユニットは結合によって近接するまで機能しません。標識されたウイルスタンパク質断片をSARS-CoV-2抗体を含むサンプルとインキュベートすると、抗体に結合し、SmBiTとLgBiTサブユニットが近接して機能性ルシフェラーゼを形成します。Lumit検出試薬を添加すると、発光シグナルが生成され、マイクロプレートリーダーで読み取られます。
Lumitアッセイのシンプルな「添加して読み取る」フォーマットは図1に示されています。洗浄ステップはなく、結果は1時間以内に得られるため、ハイスループットスクリーニングに適しています。SpectraMax® iD5マルチモードマイクロプレートリーダーは、超冷却型光電子増倍管(PMT)を搭載し、Lumit Dx SARS-CoV-2イムノアッセイの高感度な発光検出を提供します。
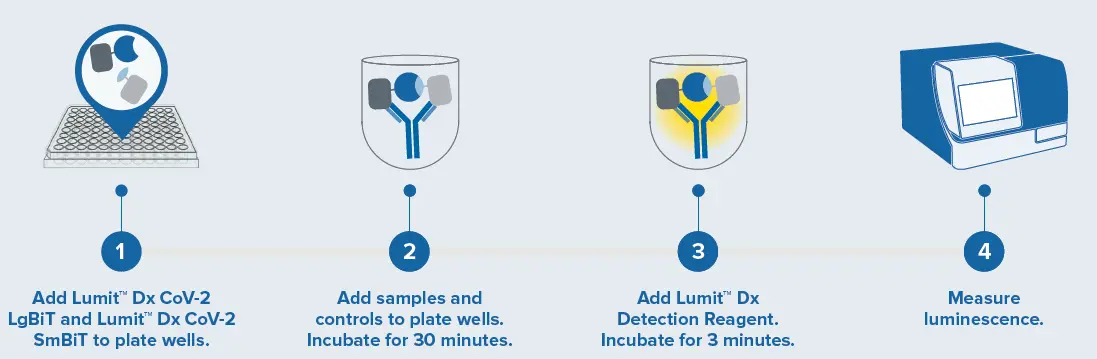
図1. Lumit Dx SARS-CoV-2イムノアッセイのワークフロー「添加-インキュベート-読み取り」フォーマットにより、結果は1時間以内に得られ、自動化およびハイスループットスクリーニングに適しています。
材料
- Lumit Dx SARS-CoV-2イムノアッセイ (プロメガ)
- COVID-19陽性血清サンプル (BioIVT)
- 正常ヒト血清(Amsbio)
- 96ウェル白色マイクロプレート(Greiner)
- SpectraMax iD5マルチモードマイクロプレートリーダー(モレキュラーデバイス)
方法
アッセイ試薬は以下の手順で調製し、プレートをセットアップしました(詳細はLumit Dx SARS-CoV-2イムノアッセイのテクニカルマニュアルをご参照ください):
- 1X Lumit-Dxイムノアッセイ希釈バッファ:10X Lumit-Dxイムノアッセイ希釈バッファ5 mLをLumit™-Dx PBS/EGTA 45 mLに加えて調製しました。
- 血清サンプルの希釈:COVID-19患者または健常ドナーの血清30 μLを1X Lumit-Dxイムノアッセイ希釈バッファ70 μLと混合しました。サンプルは三重測定に十分な量を準備しました。通常、サンプルは単一ウェルで測定し、1サンプルあたり15 μLのみ必要です。
- Lumit-Dx CoV-2 BiTsマスターミックス:使用直前に以下をチューブ内で混合しました:1X Lumit-Dxイムノアッセイ希釈バッファ5 mL、Lumit-Dx CoV-2 LgBiT(赤キャップ)9.4 μL、Lumit-Dx CoV-2 SmBiT(青キャップ)9.4 μL。チューブを軽く反転して混合しました。
- Lumit-Dxポジティブコントロール、ネガティブコントロール、アッセイキャリブレーター:使用直前に解凍し、室温に戻しました。内容物を底に集めるために短時間遠心しました。
- 96ウェル白色プレートに以下を添加しました:
⚪︎Lumit CoV-2 BiTsマスターミックス40 μL(全アッセイウェル)
⚪︎希釈した患者血清サンプル20 μL(三重測定)
⚪︎Lumit-Dxポジティブコントロール20 μL(三重測定)
⚪︎Lumit-Dxネガティブコントロール20 μL(三重測定)
⚪︎Lumit-Dxアッセイキャリブレーター20 μL(三重測定) - プレートをカバーし、室温で20分間インキュベートしました。
- インキュベーション後、Lumit-Dx検出試薬を使用直前に調製しました:1X Lumit-Dxイムノアッセイバッファ7 mLとLumit-Dx検出基質(灰色キャップ)230 μLを混合し、チューブを軽く反転して混合しました。
- 検出試薬60 μLをウェルに添加し、プレートを室温で3分間インキュベートしました。
- プレートはSpectraMax iD5プレートリーダーで、表1に示す設定を用いて測定しました。測定後、相対発光単位(RLU)はSoftMax® Proソフトウェアのプレートセクションに表示されました。プレートのウェルはテンプレートでグループに割り当てられ、結果のグループテーブルを用いて計算および表示しました。
| Parameter | Selected settings |
|---|---|
| Read mode | LUM |
| Read type | Endpoint |
| Wavelengths | All wavelengths |
| Plate type | 96-well standard opaque |
| PMT and optics |
Integration time: 1000 ms Read height: 4.7 mm |
| More settings | Show pre-read optimization |
表1. SpectraMax iD5プレートリーダーでのLumit-Dxアッセイ用装置設定 すべての波長設定(波長選択なし)が選択され、リーダーによる発光検出を最大化しました。読み取り高さは、SoftMax Proソフトウェアの「Read Height Adjustment」設定を使用して読み取り前に最適化しました。
アッセイの品質管理は、キットのテクニカルマニュアルに記載されている方法で評価しました。Lumit-Dxアッセイキャリブレーターに加え、Lumit-Dxポジティブコントロールおよびネガティブコントロールを使用して、アッセイ性能を確認しました。ポジティブコントロールはキャリブレーターより高いRLUを示し、ネガティブコントロールはキャリブレーターより低いRLUを示す必要があります。これらの条件が満たされない場合、プレートの結果は無効となります。
結果
アッセイ結果は、各試験サンプル(S)の相対発光単位(RLU)をアッセイキャリブレーター(C)の平均RLUで割った比率を用いて算出しました。比率(S/C)≥ 1の場合、サンプルはSARS-CoV-2抗体陽性を示し、比率 < 1の場合、陰性を示しました。アッセイキャリブレーターの平均RLUは548であり、6つのCOVID-19患者サンプルの平均RLUは1787~14,155の範囲で、健常ドナーのRLUは86でした。
表2に示すように、COVID-19患者サンプルのすべての比率は1を超え、陽性結果を示しました。一方、健常ドナーのサンプルは比率が1未満であり、陰性結果を示しました。
| Sample | Mean ratio (S/C) | % CV | Result |
|---|---|---|---|
| COVID-19 patient 1 | 3.26 | 1.3 | Positive |
| COVID-19 patient 2 | 7.30 | 2.2 | Positive |
| COVID-19 patient 3 | 19.80 | 0.2 | Positive |
| COVID-19 patient 4 | 14.98 | 4.3 | Positive |
| COVID-19 patient 5 | 25.83 | 6.3 | Positive |
| COVID-19 patient 6 | 14.77 | 4.7 | Positive |
| Healthy donor | 0.15 | 9.5 | Negative |
| Positive control | 7.74 | 3.2 | Positive |
| Negative control | 0.25 | 5.6 | Negative |
表2. SpectraMax iD5プレートリーダーでのLumit Dx SARS-CoV-2アッセイの患者サンプル結果 すべてのサンプルおよびアッセイコントロールは三重測定で実施し、%CVを示しています。結果はSoftMax Proソフトウェアを用いて計算および解釈しました。
注記:アッセイプレートはSpectraMax i3x、SpectraMax M5、およびSpectraMax Lプレートリーダーでも読み取られ、同様の結果が得られました。
結論
ウイルスに感染またはワクチン接種を受けた多数の個人から採取したサンプルを用いて、SARS-CoV-2に対する免疫応答のタイミングと持続期間を解明するため、SARS-CoV-2抗体の血清サンプルを大量に迅速に検査する必要があります。Lumit Dx SARS-CoV-2イムノアッセイは、研究者に迅速な結果を得るためのシンプルなワークフローを提供します。SpectraMax iD5プレートリーダーおよびSoftMax Proソフトウェアと組み合わせて使用することで、結果の計算と解釈が自動化され、より少ない手作業で高スループットを実現できます。
PDF版(英語)