Application Note ClonePixとCloneSelect Imagerで
ウイルス特異的ハイブリドーマ開発を強化
- 希少で高分泌のクローンを見つける確率を高めるため、従来法より多くのクローンをスクリーニングします
- 独自のプロセスにより、力価レベルが向上したハイブリドーマを作製します
- 最適な産生細胞を見つける確率を高めます
PDF版(英語)
はじめに
二本鎖DNA(ds-DNA)ウイルスはヒトにさまざまな疾患を引き起こします。ヘルペスウイルス目やアデノウイルス科、パピローマウイルス科に属する種は、類似した症状を示すことがあります。さらに、ウイルス特異的な診断を血清学的またはタンパク質ベースで確認することは、ウイルスゲノム内の抗原保存性により複雑になる場合があります。高いプロテオーム相同性や血清間の交差反応性は、個々のds-DNAウイルス種の識別を困難にします。本研究の目的は、バイオ医薬品開発に使用するため、交差反応性のない高特異性モノクローナル抗体を分泌する最適な産生細胞株を同定することでした。
ClonePix™システムは、親ハイブリドーマ材料からサブクローン化された数百のコロニーをハイスループットでスクリーニングするために使用されました(従来の親株の収量はmAbで1 mg/L未満でした)。生存性が高くIgG分泌量の多いクローンは、CloneSelect™ Imager技術を用いて増殖特性を客観的に評価しました。この高効率な自動クローン選択により、免疫原性ウイルス抗原に対して高特異性抗体を産生する高力価ハイブリドーマ細胞株の救済と安定化が可能になりました。これらの技術の組み合わせにより、免疫診断デバイス開発に十分な材料が得られました。
材料
- ClonePix®システム(モレキュラーデバイス)
- CloneSelect Imager(モレキュラーデバイス)
- ハイブリドーマ/ミエローマ用CloneMedia半固形培地(モレキュラーデバイス)
- CloneDetect Reagent, Mouse IgG (H+L) Specific, Fluorescein(モレキュラーデバイス)
低産生ハイブリドーマの救済
従来のハイブリドーマ開発法では、目的抗原で免疫した宿主動物の脾細胞とミエローマ細胞株を化学的に融合させます。融合したハイブリドーマは、希釈法による選択とELISAスクリーニングを経て、抗原特異的モノクローナルハイブリドーマ株を限られた数だけ分離します。この方法は最大30週間に及ぶ長期間と多くの操作を要し、得られる細胞株は力価が低く、細胞株の活力や生産性を正確に把握することは困難でした。
最初のds-DNAウイルス特異的ハイブリドーマ細胞株は1990年代に希釈法で開発されましたが、モノクロナリティや安定性は最適化されていませんでした。長年にわたり、さまざまな血清や培地組成で静置培養やローラー培養を繰り返しましたが、クローンは不安定なままでした(図1)。さらに、抗体収量は3 mg/Lを超えることはなく、精製IgGの品質も均一ではなく、調製物には凝集が認められました。
本研究の目標は、より高力価の抗体を産生する親株をサブクローン化することで、特定のハイブリドーマ細胞株を救済し安定化することでした。ClonePixプラットフォームは、メチルセルロース半固体培地とCloneDetect試薬によるラベルフリー検出を利用し、過去に融合した多数のハイブリドーマを再スクリーニングするという大きな技術的利点を提供します(図2)。
ClonePixシステムを用いたハイスループットスクリーニングにより、低産生の親クローンから安定した高産生クローンを救済することができました。

図1. 親ハイブリドーマ細胞株におけるIgG分泌の可視化は、ds-DNAウイルス特異的抗体を産生しているのはわずか約7%であることを示唆しています。ハイブリドーマ細胞はCloneMedia半固体培地に200 cells/mLで播種されました。蛍光標識CloneDetect試薬を添加し、分泌IgGのin situ検出を可能にしました。コロニーはClonePixシステムで白色光150 ms(A)および蛍光500 ms(B)でイメージングしました。FITCシグナルの変動は、親株が不安定で非モノクローナルであることを示しています。
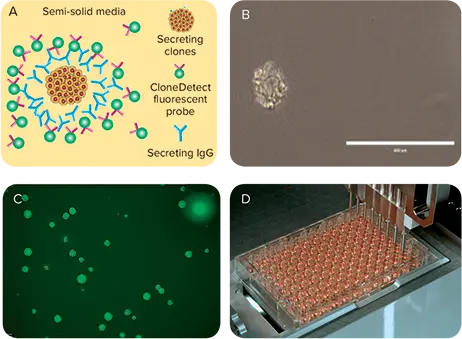
図2. ClonePix技術の原理。A:メチルセルロースマトリックス中で成長する個々のハイブリドーマクローンからの抗体検出の概念図。B:成長中のハイブリドーマクローン周囲に沈殿した抗体の白色光画像。C:ClonePixシステムによるターゲットクローンの検出と選択。D:ClonePixシステムによるターゲットクローンの自動ピッキングと移送。
高力価クローンの迅速な単離
ClonePixシステムは、ワークフローの生産性とコスト効率を大幅に改善し、希少な高分泌クローンを見つける確率を高めることで、モノクローナル抗体生成に要する時間を従来の希釈法と比較して最大50%短縮します。
このプロセスでは、親ハイブリドーマクローンを拡大培養し、ClonePixシステムで目的クローンを解析・ピッキングしました。FITC標識CloneDetect試薬を用いてクローンを撮像し、ClonePixソフトウェアで蛍光強度を解析しました。FITC陽性クローンは外部平均強度[FITC]値に基づいてランク付けされ、選択されました。全体で480のFITC-IgG陽性クローンがピッキングされ、これはスクリーニングした親クローン全体のわずか5~6%に相当します。高分泌クローンの大部分は小型(40~60細胞)であり、大型で増殖の速いクローン(70~150細胞)はIgG分泌陰性と判定されました(図3)。
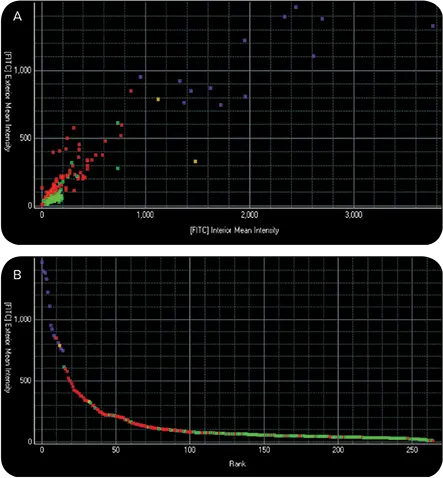
図3. ClonePixソフトウェア解析による生存性の高い高分泌コロニーの検出と選択。A:散布図は外部および内部平均強度の間に線形相関があることを示し、IgGが適切に分泌されていることを示唆します。低IgG産生クローンは不均一な集団に起因します。B:ランキングプロットは紫色で選択されたクローンを示します。カットオフはFITCシグナルで、外部700以上、内部1000以上のクローンを選択しました。
480の高分泌クローンはCloneMedia半固体培地からピッキングされ、液体クローニング培地200 µLを含む5枚の96ウェルプレートに移送され、3日間培養されました。CloneSelect Imagerを用いて96ウェルプレート内のクローンを撮像し、細胞増殖を客観的かつ定量的に評価しました。優れた撮像速度(96ウェルプレートあたり90秒未満)により、5日間にわたりコロニー増殖を迅速にモニタリングできました。このプロセスにより、146のトップグロワーが単離されました(図4)。
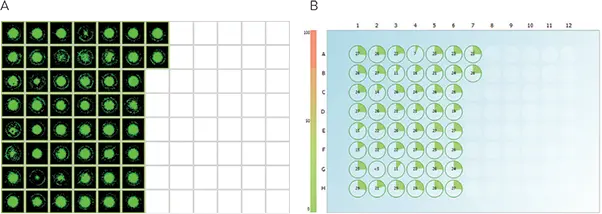
図4. CloneSelect Imagerソフトウェア解析により最適な増殖クローンを識別 480ピックのサブセットの画像解析は、コロニーの細胞形態と増殖特性(A)、各ウェルのコロニー数と面積の推定(B)を示し、効率的な増殖追跡を可能にします。増殖の遅いコロニーは除外され、トップグロワー(全体の30%、146コロニー)がペプチドアッセイで特異性をスクリーニングするために使用されました。
サブクローンのスクリーニングとパイロットスケール解析
146のトップグロワーは、mAb結合エピトープを表す合成ペプチドで抗原特異性をスクリーニングしました。ペプチドは抗体に対して強い親和性を示すことが以前の研究で確認されており、高親和性抗体を分泌する新規サブクローンのスクリーニングに使用されました。
ビオチン化ペプチドをストレプトアビジン表面に固定し、146サンプルのハイブリドーマ未希釈上清を添加してIgG結合を測定しました。最も特異性の高い7つのサブクローンが選択され、バンキングされました。
高IgG分泌サブクローンのパイロットスケール生産
7つの高価値で特異性の高いサブクローンは液体培養でスケールアップされ、将来の解析に備えました。十分な培養量が得られた後、5つのサブクローンは将来の参照研究用に凍結され、残りの2つの高結合・高IgG分泌クローンは2~3週間拡大培養され、1リットルのパイロットスケール生産が完了しました。
生産不良のハイブリドーマをレスキューするワークフロー
ds-DNAウイルス特異的抗体の診断開発を進めるため、ClonePix技術(CloneMatrix半固体培地およびFITC標識CloneDetect試薬を含む)を用いて480のFITC陽性ハイブリドーマクローンをスクリーニングしました。CloneSelect Imagerで同定された146の最速増殖クローンのうち、7つの高産生クローンがターゲットペプチド結合に対して高特異性を示しました。2つのサブクローンがパイロット生産と細胞バンキングに選択されました。このワークフローはハイブリドーマスクリーニング時間を最大50%短縮し、追加研究や生産に適した堅牢な候補を選択します。
モノクロナリティとIgG分泌の均一性確認
ClonePixシステムによる再クローニングと特異性確認後、2つのサブクローンはCloneMedia半固体培地に200 cells/mLで再播種され、CloneDetect試薬を添加しました。ClonePixシステムソフトウェアによる可視化と解析は、IgGが適切に分泌されており、均一な分泌細胞集団により高IgG収量が得られていることを示しました(図5)。
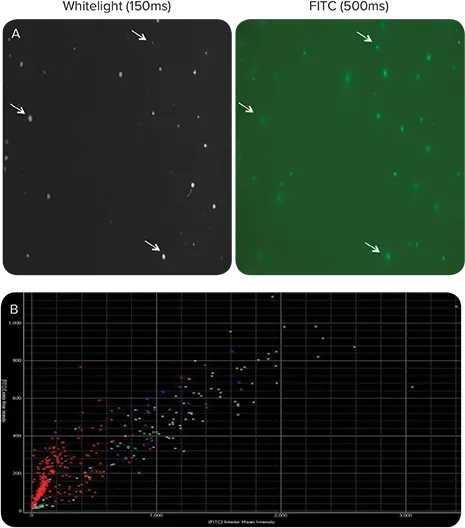
図5. ClonePixによる親ハイブリドーマのサブクローン化は、より高い収量で均一なIgG分泌を実現します サブクローンのデータサブセットを示します。A:サブクローン化によりFITC陽性コロニーの割合が大幅に改善されました。B:散布図は外部および内部平均強度の線形相関を示し、均一性が向上していることを示します。
新規ds-DNAウイルスハイブリドーマサブクローンの生産能力
ClonePix技術を利用することで、低産生の親クローンを再スクリーニングし、高産生で安定したサブクローンを救済しました。mAbはProtein Gカラムで精製され、総収量が定量化されました。両方の新規サブクローンは、親クローンの過去の収量(約1 mg/L)と比較してIgG生産量が劇的に改善し、17~25 mg/Lを示しました(図6)。
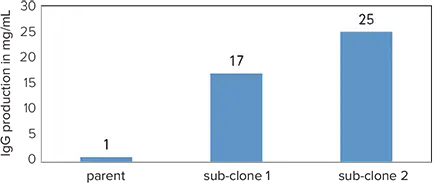
図6. ds-DNAウイルスIgGクローンの生産能力 ClonePixシステムによるサブクローン化は、細胞株の力価を劇的に増加させました。
結論
ClonePix技術は、手動操作を減らしながらスクリーニングされたハイブリドーマサブクローンのタイムラインと品質を改善します。CloneMatrix培地とCloneDetect試薬は、分泌クローンの増殖と高感度検出を可能にします。ClonePixシステムのデータは、親クローンの低生産能力が、抗体産生細胞の小集団が高速増殖の非産生細胞に置き換えられたことに起因することを示唆しています。
CloneSelect Imagerと併用することで、ClonePixシステムは、親株の過去の生産試行(0.5~1 mg/L)と比較して、著しく高い抗体生産能力(17~25 mg/L)を持つ2つの高収量・高親和性ハイブリドーマサブクローンを特定する強力なツールであることが証明されました。この技術は、特定のds-DNAウイルスを検出する新規治療用抗体の開発に効果的に貢献します。
詳しくはCloneSelect Imager をご覧ください >>
PDF版(英語)