Application Note 汚染牛トランスフェリンアッセイ
PDF版(英語)
はじめに
牛トランスフェリンは76,000ダルトンの糖タンパク質で、牛血清の構成成分の一つです。血清中に含まれるトランスフェリンは鉄イオンと結合していることがあります。鉄飽和型はホロトランスフェリンと呼ばれ、鉄欠乏型はアポトランスフェリンと呼ばれます。通常の血清には、鉄の飽和度が異なるすべての形態のトランスフェリンが封じ込められます。ウシ・トランスフェリンを封じ込めた子牛胎児血清は、組換え医薬品の製造のための哺乳類細胞培養培地に使用することができます。組換え医薬品の精製プロセスにおいて、ウシトランスフェリンは生成タンパク質と共精製される可能性があり、臨床使用において生物学的危険性を示す可能性があります。したがって、哺乳動物細胞に由来する最終製品中の混入ウシトランスフェリンをアッセイすることが必要な場合があります。ウシトランスフェリンのアッセイ法は、プロセス全体を通して製品の精製をモニターするためにも使用できます。
このアプリケーションノートでは、市販の抗ウシトランスフェリン抗体を用いたウシトランスフェリンアッセイの予備的なプロトコールと性能試験について説明します。このノートはガイドとして作成されたものであり、このアッセイのバリデーションを示すものではなく、また必ずしも最適な性能パラメータを説明するものではありません。
材料
注:ILA キットに含まれる Assay Buffer Concentrate は、コンタミヒトトランスフェリンアッセイでは一切使用しません。
- Molecular Devices Corporation(カタログ番号 0200-0500)の Threshold® System(1311 Orleans Drive, Sunnyvale, CA 94089, tel: 408-747-1700 または 800-635-5577)。
- Molecular Devices CorporationのImmuno-Ligand Assay Labeling Kit(カタログ番号R9002)。
- Molecular Devices CorporationのImmuno-Ligand Assay Detection Kit(カタログ番号R9003)。
- BSA フリーアッセイバッファー。
- ILA キットに含まれる濃縮アッセイバッファーにはウシ血清アルブミン(BSA)が封入されています。緩衝液の調製に使用される BSA は高品位ですが、アッセイに影響を及ぼす可能性のあるトランスフェリンが封じ込められ ている可能性があります。ヒトトランスフェリンアッセイにはBSAを含まないアッセイバッファーが使用されます。BSAを含まないアッセイバッファーの処方は以下の通りです:
| 10X ストック(1 リットル) | 1X 最終濃度 | |
|---|---|---|
| KH 2 P0 4 |
4.08 g | 3.0 mM |
| K 2 HP0 4 |
12.19 g | 7.0 mM |
| NaCl | 87.7 g | 150 mM |
| NaN 3 |
0.5 g | 0.005% (w/v) |
| トリトンX-100 | 2.5 mL | 0.025% (v/v) |
| pH | 6.5 | 7.0 |
表 1: BSA フリーアッセイバッファーの調合。
- BSA フリーアッセイバッファーの 10 倍溶液を脱イオン水で 1:10 に希釈したものを 500 mL 調製し、0.22 µm のフィルターでろ過します。10X ストックは 4℃で保存する。結晶が生じた場合は、室温に温め、結晶を溶解してから 1X 溶液を調製します。バッファーへのコンタミネーションを防ぐため、滅菌済みピペットチップと脱イオン水でよく洗ったガラス器具を個別に包装したもののみを使用します。
- 牛トランスフェリン(各種形態の混合物)は、ニュージャージー州ホープウェルのInter-Cell Technologies Inc.から購入しました(Tel: 609-466-4766)。牛トランスフェリンの別の供給源も試験されました(JRH Biosciencesによるアポ型とホロ型):トランスフェリンの異なる供給源は「アッセイの特徴」で比較されています。Inter-Cell Technologies 社のウシトランスフェリンは、トランスフェリンの混合型を含有しているため、本アプリケーションノートでは標準抗原として使用します。
- ベシル・ラボラトリーズ社のヒツジ抗ウシ・トランスフェリン親和性精製ポリクローナル抗体(カタログ番号A10-122A)Montgomery, Texas, tel: 409- 597-6111。その他の抗体も試験しました(Inter-Cell Technologies, Inc.のウサギ抗ウシトランスフェリンのIgG画分、Accurate Chemical & Scientific Corp.のウサギ抗ウシトランスフェリンのIgG画分)。Bethyl Labのヒツジ抗体は、バックグラウンドシグナルが最も低く、最も良好な反応を示しました。
- シグマ・ケミカル社のオバルブミン(カタログ番号A-5503)。
- ファルマシアバイオテック社のSephadex® G-25カラム(PD-10、カタログ番号17-0851- 01)。
- サンプルは、Molecular Devices Corporationの顧客のご厚意によりご提供いただきました。
方法
抗体の標識
ヒツジ抗ウシトランスフェリン抗体は、Threshold System Operator's Manual の ILA セクションおよび ILA アプリケーションノート Optimizing the labeling of proteins に記載されている方法で標識しました。
ヒツジ抗ウシトランスフェリン抗体は、防腐剤を含むリン酸緩衝液中で供給されます。そのため、標識の前に抗体をPBS(10 mMリン酸塩、150 mM NaCl、pH 7.0)に対して透析しました。DNP-ビオチン-NHSおよびフルオレセイン-NHSハプテンを250μgの抗体と別々に、遮光して室温で2時間インキュベートしました。モルカップリング比(MCR)は、タンパク質1モルあたりインキュベートされたビオチンまたはフルオレセインのモル数として定義されます。使用したMCRは、フルオレセインが20:1、ビオチンが30:1でした。
25mLのPBSで平衡化したPharmacia PD-10カラムに反応混合物を通すことにより、未反応のハプテンを抗体から分離しました。タンパク質濃度、タンパク質回収率、モル取り込み比(MIR)は、Threshold System Operator's ManualのILAセクションに記載されているように計算しました。MIR は、タンパク質 1 モルあたり共有結合したハプテンの平均モル数として定義されます。表 2 に、3 つの独立した標識反応で得られたモル取り込み比を示します。抗体のストック濃度は約1 mg/mLでした。
| 標識# | MIR ビオチン/Ab | MIR フルオレセイン/Ab |
|---|---|---|
| 1 | 3.8 | 3.6 |
| 2 | 3.1 | 3.5 |
| 3 | 3.0 | 3.6 |
表2:4種類の標識で得られたモル導入率
標識後、抗体を BSA 不要の Assay Buffer で 20 µg/mL に希釈し、担体タンパク質として 1 mg/mL のオバルブミンを加えました。150μLのアリコートをSarstedt滅菌チューブに入れて-20℃で保存しました。
試験あたりの最適抗体濃度の決定(ローディング試験)
3つの濃度のビオチン化および蛍光標識抗ウシトランスフェリン抗体を、3つの濃度のウシトランスフェリン(0、1および10 ng/mL)と共に試験し(20、40および60 ng/test、試験濃度あたりのビオチン化および蛍光標識抗体の量は等量)、バックグラウンド率と "傾き "を評価しました。傾きとは、抗原濃度の変化に対するシグナルの変化を測定したものです。サンドイッチ形式と連続インキュベーションプロトコルを使用しました(Threshold System Operator's Manual の ILA セクションを参照)。
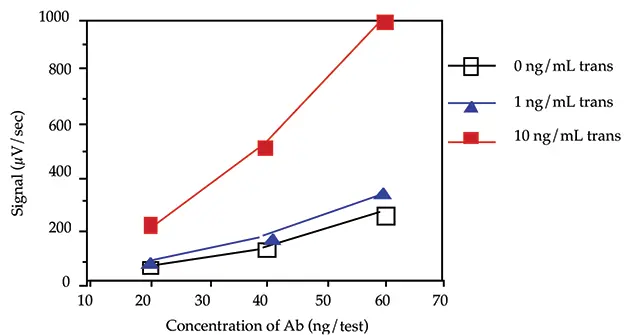
図 1. 負荷試験。
図 1 は、40 ng/test(400 ng/mL)のビオチン化抗体と 40 ng/test(400 ng/mL)の蛍光化抗体の濃度により、許容可能なバックグラウンドシグナル(0 pg/mL ウシ トランスフェリンの場合)と、ウシ トランスフェリン存在下(1 および 10 ng/mL ウシ トランスフェリン)で満足できる率が得られたことを示しています。このアプリケーションノートの残りの実験では、40 ng/testの抗体濃度を使用しました。
アッセイプロトコル
ステップ 1 ポリプロピレンチューブに牛トランスフェリン標準曲線を調製します。牛トランスフェリン標準物質(Inter-Cell Technologies 社製牛トランスフェリンのストック濃度 2~3 mg/mL) を BSA を含まないアッセイバッファーで連続希釈します。標準品は 100 ng/mL から 1 ng/mL のウシ・トランスフェリンです。推奨される標準濃度は、100、50、20、10、5、2、1および0 ng/mLのウシ・トランスフェリンです。トランスフェリンの標準濃度は、BCAのような非特異的タンパク質アッセイまたは分光光度測定によって確認することができます。1%溶液の280nmにおける消衰係数はアポトランスフェリンで約11、ホロトランスフェリンで約14です。インターセルのトランスフェリンの濃度を測定するには、平均消光係数12.5を使用しました。
ステップ 2 必要に応じて、サンプルをポリプロピレンチューブに入れ、BSAフリーのアッセイ緩衝液で希釈します。
ステップ 3 ビオチン化抗体と蛍光標識抗体をそれぞれ40 ng/test(400ng/mL)の濃度でBSAフリーのAssay Bufferに溶解した混合液をポリプロピレンチューブに調製します。
ステップ 4 牛トランスフェリン標準品および検体を 100μL ずつポリプロピレンチューブに分注します。
ステップ5 ステップ3で調製した抗体100μLを、エッペンドルフのリピーターピペッターとCombitip® を用いてチューブに分注します。
ステップ6 チューブをパラフィルムで覆い、室温で2時間インキュベートします。
ステップ 7 BSAフリーのアッセイバッファー25 mLでキャプチャー試薬を再構成します。回収試薬を BSA フリーアッセイバッファーで 1:10 に希釈します(回収試薬 1 容量+BSA フリーアッセイバッファー 9 容量)。インキュベーションが終了したら、希釈した Capture Reagent 1 mL をエッペンドルフのピペッターと Combitip を用いて各チューブに分注します。
ステップ 8 反応混合物をろ過ユニットに移します。フィルターベースとフィルターブロックは新品でも再使用でもかまいません(洗浄方法についてはILA検出キットの添付文書を参照)。低真空でフィルタリングします。
ステップ 9 フィルタリングの間に、酵素試薬を 4 mL の BSA フリーアッセイバッファーで再構成します。再構成した酵素試薬の 1:10 希釈液を調製します(酵素試薬 1 容量+BSA フリーアッセイバッファー 9 容量)。
ステップ 10 フィルタリングユニットのウェルが空になったら、各ウェルに Wash Buffer を 2 mL ずつ分注し、高真空でフィルタリングします。真空を切ります。
ステップ 11 希釈した酵素試薬をエッペンドルフのリピーターピペッターとコンビティップを使って各ウェルに 1 mL ずつ分注し、低真空でろ過します。
ステップ 12 ろ過ユニットのウェルが空になったら、各ウェルに洗浄液を 2 mL ずつ分注し、高真空でろ過します。真空を止め、スティックを読み取ります。
アッセイ特性評価
標準曲線
標準曲線の最低キャリブレーター(1 ng/mL)は、バックグラウンドシグナルに対して30~50μV/秒のシグナルの増加を生じるウシ・トランスフェリンの濃度を計算することにより選択しました。この計算は負荷試験の結果に基づいて行われました(Threshold System Operator's ManualのILAセクションのSandwich Assay Optimizationを参照)。標準曲線の他のキャリブレーターは、最低キャリブレーターの 2 log(100倍)上の範囲に分布させました。二次方程式がデータに最もよく当てはまります(図 2 参照)。
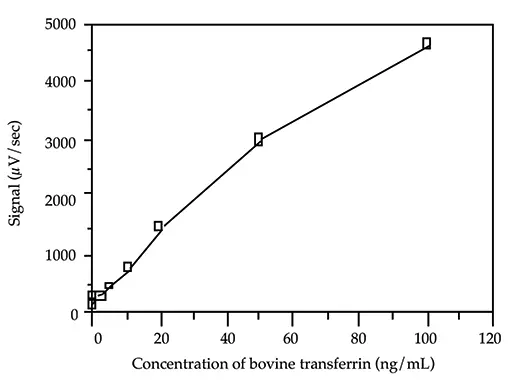
図2. 牛トランスフェリン標準曲線。
Inter-Cell 製のウシ・トランスフェリンを JRH 製のアポおよびホロ・トランスフェリンと比較しました(図 3 参照)。ストック濃度は分光光度計で確認しました。インターセルとJRHのトランスフェリンは、低濃度では同等でした。50 ng/mLでは、JRHのトランスフェリンはInter-Cellのトランスフェリンより35%高いシグナルを示しました。JRHトランスフェリンのアポ型とホロ型は同等の反応を示しました。
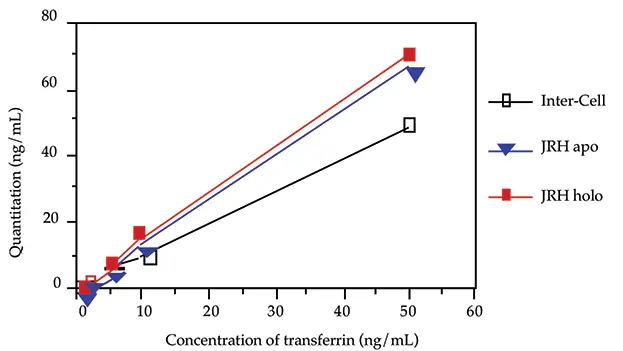
図3. 3種類のトランスフェリンの比較。
インキュベーション時間
最適なインキュベーション時間を決定するためにカイネティック研究を行いました。4種類の濃度のウシ・トランスフェリン(20、5、1、0 ng/mL)を標識抗体とともに4時間、2時間、1時間インキュベートしました。
4時間、2時間、1時間のインキュベーションでは、同様のバックグラウンドシグナルが生じました。図4は、インキュベーション時間が長くなるにつれて勾配の増加が観察されたことを示しています。インキュベーション時間を2時間以上にすることで、アッセイの感度を向上させることができます。
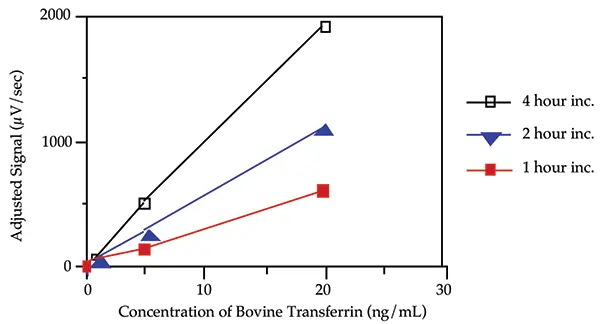
図4. インキュベーション時間の影響
検出限界
検出限界の評価についてはThreshold System Operator's Manualを参照してください。この牛トランスフェリンアッセイでは、通常1 ng/mLの牛トランスフェリンをバックグラウンドから4標準偏差の分離で検出することができます(データは示していません)。
アプリケーション
本アッセイの性能は、牛トランスフェリン含量について異なるタンパク質サンプルを試験することにより評価しました。サンプルはノンスパイクおよび既知濃度の牛トランスフェリンをスパイクして試験し、スパイク回収率(SR)は以下のように計算しました:
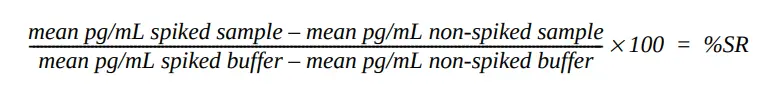
許容可能なスパイク回収率は100%+20%と定義されます。許容可能なスパイク回収率は、検体が牛トランスフェリンの測定に干渉せず、検体中の牛トランスフェリンの定量が正確であることを意味します。
BSAサンプル
BSAが緩衝液や培地の調製に使用されている場合、トランスフェリン濃度が注目されることがあります。BSAの3つの供給源について、汚染ウシトランスフェリンについて検査しました。元のサンプル濃度は365 µg/mL(サプライヤー#1)、713 µg/mL(サプライヤー#2)、937 µg/mL(サプライヤー#3)でした。3つのBSAサンプルはすべて、非スパイクおよび約15 ng/mLの牛トランスフェリンをスパイクして検査されました。BSA溶液#1および#2は非希釈および1:2希釈で試験し、BSA溶液#3は1x10-3および5x10-3希釈で試験しました。
| サンプル |
スパイク (pg/mL) |
非スパイク (pg/mL) |
ネットスパイク (pg/mL) |
実測値 (ng/mg BSA) |
%スパイク回収率 |
|---|---|---|---|---|---|
|
BSAフリーアッセイ バッファー |
12.5 | 0.4 | 12.1 | ||
|
BSAサプライヤー #1原液 |
33.9 | 19.8 | 14.1 | 54.2 | 117% |
| 1:2希釈 | 23.8 | 9.6 | 14.2 | 52.6 | 117% |
|
BSAサプライヤー #2 原液 |
19.7 | 8.2 | 11.5 | 11.5 | 95% |
| 1:2希釈液 | 16.2 | 5.2 | 11.0 | 14.6 | 91% |
|
BSAサプライヤー #3 原液 |
25.8 | 11.8 | 14.0 | 12,600 | 116% |
| 5×10-3希釈液 | 18.0 | 6.0 | 12.0 | 12,800 | 99% |
表3: 牛トランスフェリンアッセイプロトコルを用いたBSA溶液の結果。
BSA溶液中の汚染トランスフェリン濃度は、サプライヤー#1ではBSA 1 mgあたり53.4 ng、サプライヤー#2ではBSA 1 mgあたり13.1 ng、サプライヤー#3ではBSA 1 mgあたり12,700 ngでした。牛トランスフェリンアッセイにより、3つの異なる業者のBSA純度を比較することができます。
子牛胎児血清
子牛胎児血清のウシトランスフェリン検査を行いました。子牛胎児血清中のウシ・トランスフェリンを定量することは、血清が細胞培養培地の調製に使用される場合、興味深いかもしれません。試験した各希釈液(2x10-5~1x10-7)は、ノンスパイクまたは約20ng/mLのウシトランスフェリンをスパイクして試験しました。
| サンプル |
スパイク (ng/mL) |
スパイクなし (ng/mL) |
ネットスパイク (ng/mL) |
実測値 (ng/mL BSA) |
スパイク回収率 |
|---|---|---|---|---|---|
|
BSA フリー アッセイバッファー |
18.7 | 0.2 | 18.5 | ||
|
2x10 -5 希釈
|
– * |
136.9 | - | - | - |
|
1x10 -5 希釈
|
71.3 | 47.6 | 23.7 | 4.8 | 128% |
|
5x10 -6 希釈
|
43.3 | 22.3 | 21.0 | 4.5 | 114% |
|
1x10 -6 希釈
|
21.8 | 5.3 | 16.5 | 5.3 | 89% |
|
2x10 -7 希釈
|
18.2 | 0.8** | 17.4 | - | 94% |
|
1x10 -7 希釈
|
20.1 | 0.9** | 19.2 | - | 104% |
表4:ウシ・トランスフェリン測定プロトコルを用いた子牛胎児血清溶液の測定結果。
(*) シグナルが高すぎて標準曲線から定量できません。(**) 検出限界以下。
試験した子牛胎児血清は、5x10-6および1x10-6希釈で許容可能なスパイク回収が可能であり、これらの希釈から得られたデータに基づき、平均4.9 mg/mLのウシ・トランスフェリンを封じ込めました。
マウスIgGサンプル
マウスIgG1サンプルを、約15 ng/mLのウシトランスフェリンのスパイクの有無にかかわらず、汚染ウシトランスフェリンについて検査しました(原液および1:2希釈)。元のサンプル濃度は 14 mg/mL マウス IgG1 でした。
| サンプル |
スパイク (ng/mL) |
スパイクなし (ng/mL) |
ネットスパイク (ng/mL) |
実測値 (pg/mg Mu IgG 1 ) |
%スパイク回収率 |
|---|---|---|---|---|---|
|
BSA フリー アッセイバッファー |
12.7 | 0 | 12.7 | ||
|
マウスIgG 1 1:50 |
24.5 | 10.1 | 14.4 | 721 | 113% |
|
マウスIgG 1 1:100 |
18.3 | 4.7 | 13.6 | 671 | 107% |
表 5: ウシトランスフェリンアッセイプロトコルを用いたマウス IgG1 サンプルの結果。
希釈サンプルと非希釈サンプルの平均値から、テストしたサンプルは十分なスパイク回収が可能であり、マウス IgG1 1 mg あたり 696 pg の汚染ウシ トランスフェリンを封じ込めました。
アッセイ精度
マウスIgG1サンプル(14 mg/mL)を5日間トリプリケートし、日ごとの再現性を調べました。同じ実験における再現性は、5 つの複製を試験することで調べました。以下の表に得られた結果を示します。
| アッセイ内再現性 | 日間再現性 | ||
|---|---|---|---|
| 日間 |
定量 (ng bov. IgG/mL) |
日間 |
定量 (ng bov. IgG/mL) |
| 1 | 10.0 | 1 | 10.3 |
| 10.7 | 2 | 10.1 | |
| 10.2 | 3 | 10.6 | |
| 9.4 | 4 | 9.6 | |
| 10.3 | 5 | 11.1 | |
| 平均 | 10.1 | 平均 | 10.3 |
| 標準偏差 | 0.5 | 標準偏差 | 0.6 |
| C.V. | 4.7% | C.V. | 5.4% |
表6: 牛トランスフェリン測定法の再現性と繰り返し性。各値は3反復の平均値。
概要
本アプリケーションノートのデータは、2 時間のインキュベーションと 40 ng/test の各標識抗ウシ トランスフェリン抗体を用いて作成されました(特記を除く)。これらの条件により、ダイナミックレンジは2 log(100倍)、ウシトランスフェリンの検出限界は1 ng/mLです。インキュベーション時間を短縮してより迅速なアッセイを行うことも、インキュベーション時間を長くしてより高感度なアッセイを行うこともできます。アッセイ性能のバリデーションは、試験する製品ごとに決定する必要があります。
PDF版(英語)