Application Note 3Dバイオプリント卵巣がんモデルの
イメージング特性評価
- ハイコンテントスクリーニングと一過性トランスフェクションの組み合わせは、3Dバイオプリントアッセイの特性評価と検証に役立ちます
- 一過性遺伝子発現は、3Dバイオプリントモデルの多様性を高める強力なツールです
- 複数波長解析ツールは、3Dバイオプリントモデルの性能を最大限に活用し、モデル内の異なる細胞集団間の相互作用を研究するために不可欠です
PDF版(英語)
Z. Baka, C. Godier, H. Alem | Institut Jean Lamour
R. Storm, M. Cattaneo, S. Tendil | モレキュラーデバイス
N. Chaboche, A. Nyamay’Antu | Polyplus Transfection
V. Gribova | INSERM
はじめに
3Dバイオプリンティングは、生体適合性材料と細胞を積層的に堆積させ、生物学的に機能する3D構造や人工組織モデルを構築する技術です *1。この技術は組織工学の分野に革命をもたらし、複雑で事前に設計された構造を高い再現性で作成することを可能にしました。これまでに、軟骨 *2、骨 *3、皮膚再生 *4など、さまざまな組織工学に基づく3Dバイオプリンティングのアプローチが報告されています。また、この技術は新しい前臨床がんモデルの作成にも活用されています。実際、2D細胞培養モデルは予測性の欠如が問題視されており、3Dバイオプリンティングは、異なる細胞種や細胞外マトリックス由来分子を堆積させることで腫瘍微小環境(TME)をより正確に再現する代替手法として注目されています。肺がん *5、乳がん *6、膠芽腫 *7など、多くの3Dバイオプリンティングがんモデルが報告されており、スフェロイドやオルガノイドと比較して設計の柔軟性と再現性に優れています。
卵巣がんは公衆衛生上の重大な課題ですが、3Dバイオプリンティングによるモデルはまだ十分に研究されていません。この腫瘍タイプでは、がん関連線維芽細胞(CAF)ががん細胞と密接に相互作用し、がん浸潤や薬剤耐性に重要な役割を果たすことが知られています *8,*9。したがって、卵巣がんモデルを設計する際にはCAFを考慮することが不可欠です。
このアプリケーションノートでは、がん細胞(SKOV3細胞)とCAF線維芽細胞(MeWo細胞)を含む卵巣がんモデルを3Dバイオプリンティングで作成しました。SKOV3細胞はjetOPTIMUS®(Polyplus®)を用いてGFPプラスミドでトランスフェクションし、MeWo細胞はCellTracker™ Orange CMRA Dye(ThermoFisher)で染色しました。両細胞種はゼラチン-アルギン酸ベースのハイドロゲルに含められ、「バイオインク」を作成し、円柱状の腫瘍様構造を形成しました。細胞分布の均一性と再現性は、ImageXpress® Picoイメージングシステムを用いて評価しました。
結果と考察
図1に示すように、バイオプリント構造のイメージングでは、GFPを発現するSKOV3細胞と蛍光染色されたMeWo細胞がゼラチン-アルギン酸ベースのマトリックス内に均一に分布していることが確認されました(図1AおよびB)。これは、バイオインク内の均一な細胞分布が3Dバイオプリンティングにおいて重要なパラメータであるため、非常に重要です *12。また、ネイティブなTMEは複数の細胞種で構成され、互いに密接に相互作用することが知られています *13。したがって、がん細胞と間質細胞の相互作用を促進するために、in vitro腫瘍モデル構築時にこの細胞近接性を再現することが重要です。
腫瘍モデルでTMEの不均一性をより正確に模倣するためには、多くの細胞種を組み合わせる必要がありますが、各細胞種の総数と比率を制御し、再現性を確保することが求められます。ImageXpress Picoは、複数の顕微鏡画像を迅速かつ容易に取得できるため、このような制御に特に適しています。CellReporterXpressソフトウェアは、Zスタック最大投影を使用して厚いサンプル内でも複数の細胞集団を定量化できます。本アプリケーションノートでは、このシステムを用いてバイオプリント腫瘍モデルを解析し、細胞数と比率に関して良好な再現性を示しました。6つのバイオプリント構造の平均SKOV3細胞数(FITCチャンネル)は837 ± 200(標準偏差 ≤ 25%)、MeWo細胞数(TRITCチャンネル)は3264.50 ± 462(標準偏差 ≤ 15%)でした。
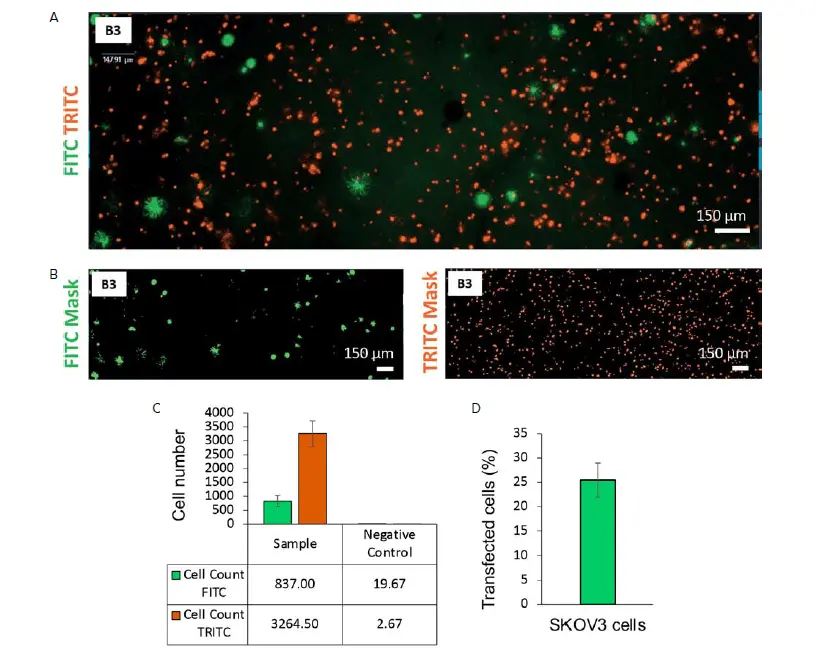
図1. GFPプラスミドでトランスフェクションしたSKOV3細胞とCellTracker Orange CMRA Dyeで染色したMeWo細胞を含む3Dバイオプリント構造の解析。 A) ImageXpress Picoシステムで取得したウェルB3の3Dバイオプリント構造のFITCおよびTRITC画像(4X、Zスタッキング)。 B) CellReporterXpressソフトウェアで作成したFITCおよびTRITC細胞カウントの解析マスク。 C) サンプル(5ウェル、染色およびトランスフェクション済み)とネガティブコントロール(3ウェル、未染色および未トランスフェクション)のFITCおよびTRITCチャンネルの平均細胞数。 D) GFPプラスミドとjetOPTIMUS-Polyplusトランスフェクションキットを用いたトランスフェクション効率の推定(FITC陽性細胞/TRITC陽性細胞の平均割合)。
このアプリケーションノートは、バイオプリント構造内で特定遺伝子の可視化が迅速に行えることを示しています。バイオプリンティング前に特定の細胞種をトランスフェクションすることで、バイオプリント構造内で一過性遺伝子発現を実現できます。これは、トランスフェクションが困難とされるスフェロイドやオルガノイドなどの他の3D細胞培養法に対する3Dバイオプリンティングの大きな利点です。本予備実験では、トランスフェクション効率の推定値は25%(標準偏差3.48%)(図1D)でした。これは、ImageXpress Picoを用いてトランスフェクションミックス濃度、DNAプラスミド量、タイミングをスクリーニングすることで改善可能です。このアプローチは、同一バイオプリント構造内で間質細胞とがん細胞の両方に対して遺伝子サイレンシングや遺伝子編集を行う可能性も提供します。
総じて、トランスフェクション、蛍光イメージング、セルカウントを組み合わせて、がん細胞とCAFを含む3Dバイオプリント卵巣腫瘍モデルの特性評価と検証を行いました。2種類の細胞の均一な分布とマトリックス内での近接性を再現でき、細胞間相互作用に有利であることを示しました。このアプローチは、染料浸透の制限を回避し、制御された再現性のある細胞分布を持つ、より複雑で完全な腫瘍モデルの作成を可能にします。3Dバイオプリント腫瘍モデルは、マイクロ流体システムへの統合前に迅速に再現性を検証でき、その後、生理学的フロー下で長期培養し、抗がん薬開発のためのよりin vivoに近い前臨床モデルを構築できます。
材料と方法
ハイドロゲル調製
必要量のゼラチンとアルギン酸ナトリウム粉末を秤量し、UV照射で1時間除染した後、10%ウシ胎児血清を添加したDulbecco’s Modified Eagle MediumとMinimum Essential Medium(MEM)の混合液に溶解しました。得られた溶液は37°Cで磁気攪拌しながら一晩保持し、完全に均質化しました。
細胞のトランスフェクションと染色
SKOV3細胞は、jetOPTIMUS(Polyplus)を用いてGFPプラスミドでトランスフェクションしました *10。適切な量のDNAをjetOPTIMUSバッファーに希釈し、適量のトランスフェクション試薬を添加しました。トランスフェクション溶液は室温で10分間保持した後、T75フラスコで60–80%コンフルエンスに達したSKOV3細胞に添加しました。
MeWo細胞は、CellTracker Orange CMRA Dye(ThermoFisher)で染色しました *11。染料をDMSOに溶解し、MEM培養液で希釈してワーキング溶液を調製しました。細胞は37°Cで30分間曝露され、その後試薬溶液を除去し、新しい完全培養液に置換しました。
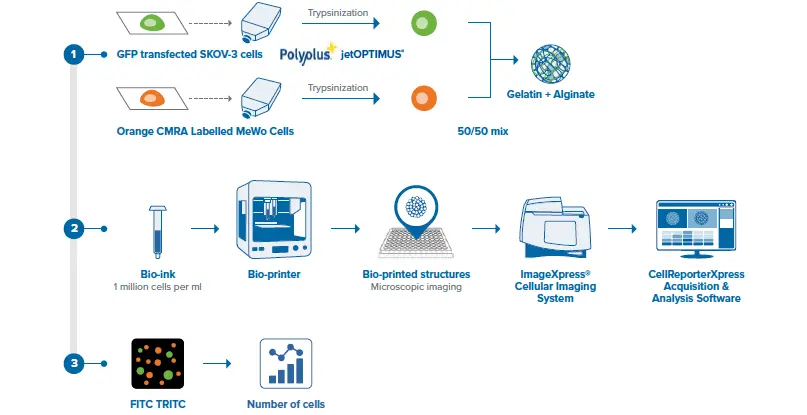
図2. 卵巣がんモデル構造のバイオプリントおよびイメージングに使用した方法の模式図
細胞カプセル化
バイオインクの調製では、トリプシン処理した細胞を新しい培養液に再懸濁し、事前に調製したポリマー溶液に慎重に添加しました。得られた懸濁液は、バイオインク内の細胞分布を均一化するためにゆっくりと撹拌しました。
バイオプリンティング工程
調製したバイオインクを3 mLカートリッジに充填し、バイオプリンティングヘッドにセットしました。バイオプリンティングは24ウェルプレートで実施しました。各3 mLカートリッジで約48構造をバイオプリントしました。バイオプリンティング後、構造は100 mM CaCl₂溶液で架橋し、新しい培養液を補充して37°C、5% CO₂で実験に必要となるまで培養しました。
細胞イメージング
バイオプリント構造を96ウェルプレート(Greiner 655892、ガラス底、黒壁)に移しました。
細胞はImageXpress Pico 自動細胞イメージングシステムを用いて4X対物レンズでイメージングしました。
画像は、各ウェルで単一サイトを透過光、FITC、TRITCチャンネルでそれぞれ5 ms、150 ms、250 msの露光時間で取得しました。4X対物レンズではウェル全体の約40%が表示されます。ハードウェアベースと画像ベースのオートフォーカスを組み合わせて、50 µm間隔で7つのZプレーンを取得しました(Zスタッキング)。最大2D投影画像はオンザフライで生成されました。
CellReporterXpress™ソフトウェアの事前設定済みセルカウント解析モジュールを使用し、FITCまたはTRITCチャンネルにシグナルを持つ細胞を定量しました。解析に使用したセグメンテーションパラメータはIntensity、最小幅、最大幅で、FITCチャンネルでは23、7、100、TRITCチャンネルでは23、7、38でした。
謝辞
Pascal Kessler – Microscopy platform of CRBS PIC-STRA, Strasbourg, France.
参考文献
- Tan B, Gan S, Wang X, Liu W, Li X. Applications of 3D bioprinting in tissue engineering: advantages, deficiencies, improvements, and future perspectives. J Mater Chem B. 2021;9(27):5385–5413. doi:10.1039/D1TB00172H
- Nguyen LH, Kudva AK, Saxena NS, Roy K. Engineering articular cartilage with spatially-varying matrix composition and mechanical properties from a single stem cell population using a multi-layered hydrogel. Biomaterials. 2011;32(29):6946–6952. doi:10.1016/j. biomaterials.2011.06.014
- Kang HW, Lee SJ, Ko IK, Kengla C, Yoo JJ, Atala A. A 3D bioprinting system to produce human scale tissue constructs with structural integrity. Nat Biotechnol. 2016;34(3):312–319. doi:10.1038/nbt.3413
- Cubo N, Garcia M, Cañizo JF del, Velasco D, Jorcano JL. 3D bioprinting of functional human skin: production and in vivo analysis. Biofabrication. 2016;9(1):015006. doi:10.1088/1758-5090/9/1/015006
- Wang X, Zhang X, Dai X, et al. Tumor-like lung cancer model based on 3D bioprinting. 3 Biotech. 2018;8(12). doi:10.1007/s13205-018-1519-1
- Swaminathan S, Hamid Q, Sun W, Clyne AM. Bioprinting of 3D breast epithelial spheroids for human cancer models. Biofabrication. 2019;11(2):025003. doi:10.1088/1758-5090/aafc49
- Wang X, Li X, Ding J, et al. 3D bioprinted glioma microenvironment for glioma vascularization. J Biomed Mater Res B. Published online 2020. doi:10.1002/jbm.a.37082
- Ji Z, Tian W, Gao W, Zang R, Wang H, Yang G. Cancer-Associated Fibroblast-Derived Interleukin-8 Promotes Ovarian Cancer Cell Stemness and Malignancy Through the Notch3-Mediated Signaling. Front Cell Dev Biol. 2021;9:684505. doi:10.3389/fcell.2021.684505
- Yan H, Guo BY, Zhang S. Cancer-associated fibroblasts attenuate Cisplatin-induced apoptosis in ovarian cancer cells by promoting STAT3 signaling. Biochem Biophysl ResCommun. 2016;470(4): 947–954. doi:10.1016/j.bbrc.2016.01.131
- jetOPTIMUS® DNA Transfection Reagent. Accessed June 9, 2022. (account creation required) https://myaccount.polyplus-transfection.com/my-account-home/protocol-download/
- CellTrackerTM Orange CMRA Dye. Accessed June 8, 2022. https://www.thermofisher.com/order/catalog/product/C34551
- Bhattacharyya A, Janarthanan G, Tran HN, Ham HJ, Yoon J, Noh I. Bioink homogeneity control during 3D bioprinting of multicomponent micro/nanocomposite hydrogel for even tissue regeneration using novel twin screw extrusion system. Chem Eng J. 2021;415:128971. doi:10.1016/j.cej.2021.128971
- Anderson NM, Simon MC. The tumor microenvironment. Curr Biol. 2020;30(16):R921–R925. doi:10.1016/j.cub.2020.06.081
PDF版(英語)