Application Note ハイコンテントイメージングと
マイクロ流体による3Dがん評価系
- 自動化されたマイクロ流体制御で複雑な3Dアッセイを効率化します
- 磁性コーティングされた3D細胞モデルと自動化されたアッセイワークフローで、一般的な3Dアッセイの課題を克服します
- 分泌因子解析からハイコンテントイメージング解析まで、複数のアッセイリードアウトを測定します
PDF版(英語)
Oksana Sirenko, PhD | Applications Scientist | モレキュラーデバイス
Matthew Hammer | Applications Scientist | モレキュラーデバイス
はじめに
近年、研究や創薬開発において、生理学的に正確な3D細胞モデルの必要性が着実に高まっています。研究者は、疾患および正常な生理を理解するために、さまざまな3D細胞モデルの形成と維持を改良してきました(*1,*2)。制限要因の一つは、特に患者由来の貴重なサンプルを用いて、複雑なアッセイを容易かつ迅速に実施できるかどうかです。スフェロイドやオルガノイドの手動での処理、染色、加工は、通常、労力を要し、サンプルの破損や損失が起こりやすい作業です。さらに、ハイコンテントイメージングは、オルガノイドがウェルの端に位置したり、ウェル内で異なる位置や高さに存在するため、困難な場合があります。また、マルチウェルプレートで薬剤処理やアッセイを行う場合、サンプルごとのリードアウト数に制限があります。
こうしたプロセスを効率化し、容易にするための新しい技術が急速に開発されています。私たちは、マイクロ流体ベースの装置 Pu·MA System® 3D MAG と 3D flowchips(Protein Fluidics社)を使用し、磁性ナノ粒子でコーティングされた3D細胞モデルを用いた自動化アッセイステップを実施しました(図1)。磁性ナノ粒子 NanoShuttle™(3) でコーティングされた3D細胞モデルは、内蔵された磁石を用いてflowchipのウェルに移送され、中央に配置されました。自動化されたマイクロ流体システムにより、培地交換、化合物添加、マイクロティッシュの処理が自動で行われました。その後、ImageXpress® Micro Confocal ハイコンテントイメージングシステム(モレキュラーデバイス)を使用し、3D構造の高解像度イメージングと、スフェロイドやオルガノイドの形態および化合物の影響を特徴づけ、定量化するための高度な解析を行いました。
私たちは、以下の2種類の複雑な3Dアッセイにおける自動化ワークフローを実証しました:
- 3Dがんスフェロイドの薬剤処理、染色、および解析:HeLaスフェロイドに化合物を24~48時間処理しました。自動化された生存率染色を用いて、化合物処理の濃度応答曲線を決定しました。
- 薬剤感受性評価とバイオマーカーの免疫蛍光解析:トリプルネガティブ乳がん(TNBC)患者由来オルガノイド(PDO)(4)の薬剤応答をアッセイしました。PDOはIFマーカーで染色され、flowchip内でイメージングされました。
Pu-MAシステムと3D MAGワークフロー
Pu·MA Systemと3D flowchipsは、オルガノイドアッセイの自動化を効率化するよう設計されています。Pu·MA System 3D MAGは、標準のPu·MA System装置に3D MAGモジュールを追加したもので、磁性ナノ粒子でコーティングされた3D細胞モデルをアッセイステップ中に保護されたサンプルチャンバー内に保持することができます(図1および図2)。
3DスフェロイドのNanoShuttle処理は、Greiner Bio-One社のプロトコール(3)に従って実施しました。ここでは、このバイオプリンティングプロセスを自動化アッセイシステムと組み合わせた新しい使用例を示します。
磁化された3D細胞モデルは、直径約1 mmの磁性ロッドを含むローディングトレイを用いてflowchipに移送され、磁性ナノ粒子でコーティングされたオルガノイドの中央配置と保持を確実にしました(図2)。flowchipはインキュベーター内のシステムに設置されます。Pu·MA Systemのシステム構造と、流体を移動させるための空気圧の使用により、インキュベーター環境内でサンプルチャンバーへのガス交換が可能になります。
flowchipは、便利なマルチウェルプレートフォーマット(384ウェル間隔 SLAS/ANSI標準)で設計されており、マルチチャネルまたは自動液体分注システムに対応しています。底面は光学的に透明で、蛍光または共焦点イメージングシステムでのイメージングに適しています(図1)。さらに、磁性ナノ粒子でコーティングされた3Dモデルの位置をアッセイ全体で中央に保持できるため、すべてのサンプルウェルで同じ撮像フィールドの自動取得が容易になります。加えて、ImageXpress Micro Confocalシステムの堅牢なオートフォーカス機能により、各サンプルウェル内のスフェロイドまたはオルガノイド全体の高解像度画像を取得できます。
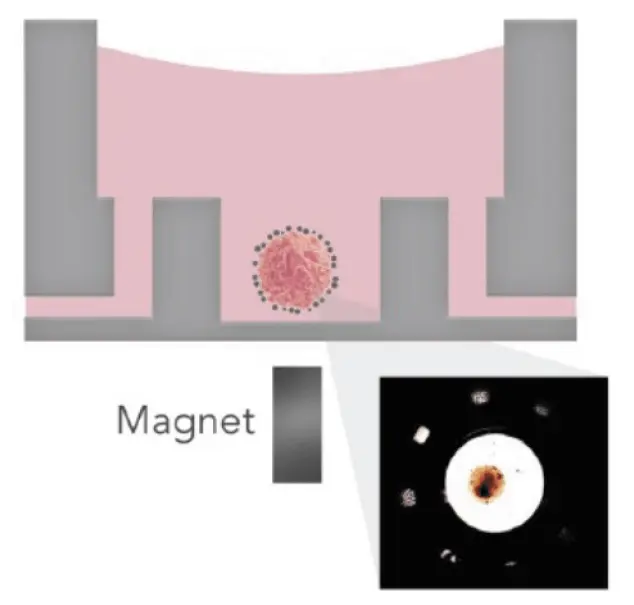
図1. Pu·MA System 3D MAG内のflowchip保護サンプルチャンバーに配置されたスフェロイドの模式図です。挿入図は、サンプルチャンバー内のNanoShuttleでコーティングされたマウスアイレットの明視野画像を示しています。
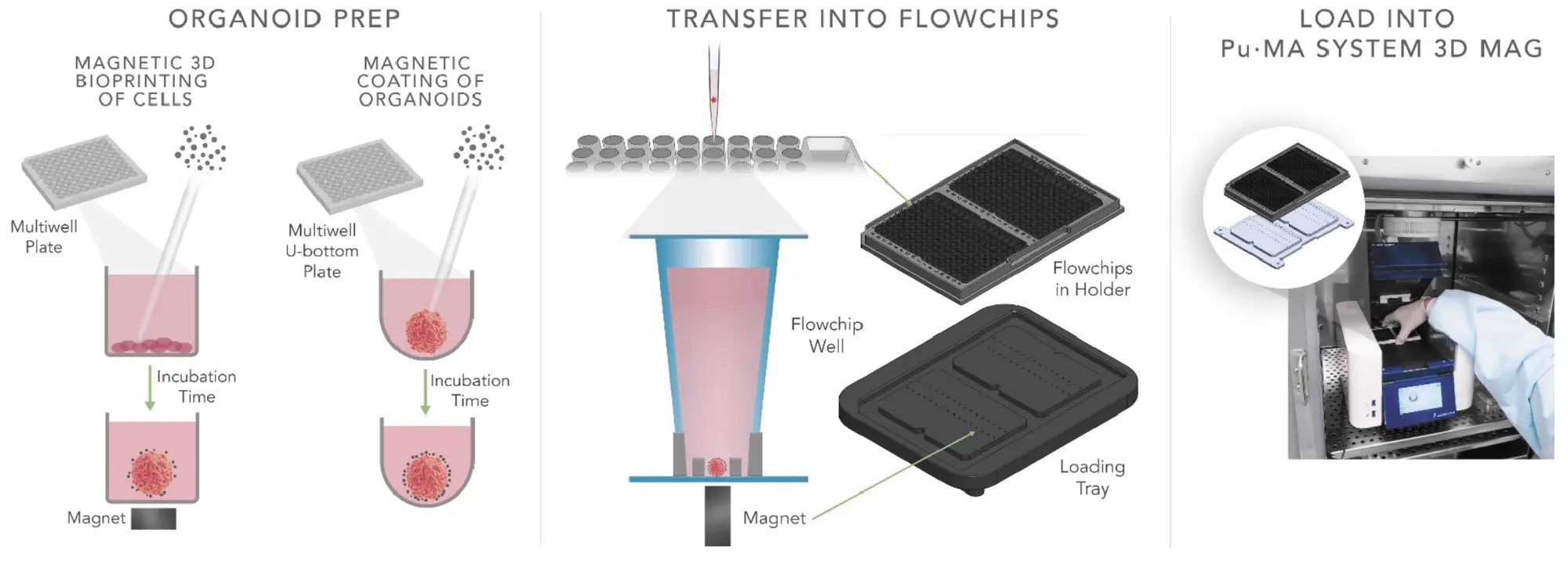
図2. 磁性コーティング、flowchipへの移送、およびPu·MA System 3D MAGへのローディングのアッセイステップです。ワークフローでは、磁性バイオプリントされた細胞に対して10,000細胞あたりNanoShuttleを1 μL使用し、事前に形成された3D細胞モデルにはサンプル(3Dマイクロティッシュ)あたり0.1 μLの比率でNanoShuttleをインキュベートしました。インキュベーション後、ローディングトレイを用いてflowchipに移送しました。試薬はサンプルウェルに隣接するウェルにロードされ、flowchipホルダーはインキュベーター内のPu·MA System 3D MAGに配置されます。自動化アッセイ完了後、flowchipはImageXpress Micro Confocalシステムに移され、ハイコンテント3Dイメージングと解析が行われました。
3Dがんスフェロイドの薬剤処理、染色、およびイメージング
このワークフローの適用例として、マイクロ流体サンプル処理と磁性ビーズを用いて、選択された細胞毒性薬剤処理によるHeLaスフェロイドの細胞生存率および細胞死を評価しました(5)。HeLa細胞は、Greiner Bio-One社のプロトコール(3)に従い、細胞非接着性384ウェルマイクロプレートにウェルあたり2,000細胞で磁性バイオプリントされました。NanoShuttleでコーティングされたHeLa細胞は、磁性保持ドライブ上で37°C、5% CO₂で1時間インキュベートされました。その後、プレートはインキュベーター内で1日保持され、形成されたスフェロイドをflowchipウェルに移送し、Pu·MA System 3D MAGで処理しました。
以下の例では、HeLa 3Dスフェロイドを異なる濃度の化合物(スタウロスポリン、0~10 μM)で22時間自動処理し、その後、培地を染色溶液に交換して2時間インキュベートしました(Calcein AM、Hoechst、Ethidium Homodimer 1)、その後PBSで洗浄しました。
処理後、flowchipは装置から取り出され、ImageXpress Micro Confocalイメージングシステムを用いてflowchip内でイメージングしました。画像は10Xまたは20X対物レンズで取得し、3D Zスタックは12~20枚の画像を510 μm間隔で撮影しました。2D投影画像はMetaXpress® ハイコンテントイメージング解析ソフトウェアのカスタムモジュールを用いて迅速に細胞生存率を定量化しました(図3)。スタウロスポリン処理後の生細胞および死細胞の数はMetaXpressソフトウェアで定量化されました。Live/Dead解析モジュールは、2D投影画像(最大投影)またはカスタムモジュールエディターを用いた3D解析に使用されました。
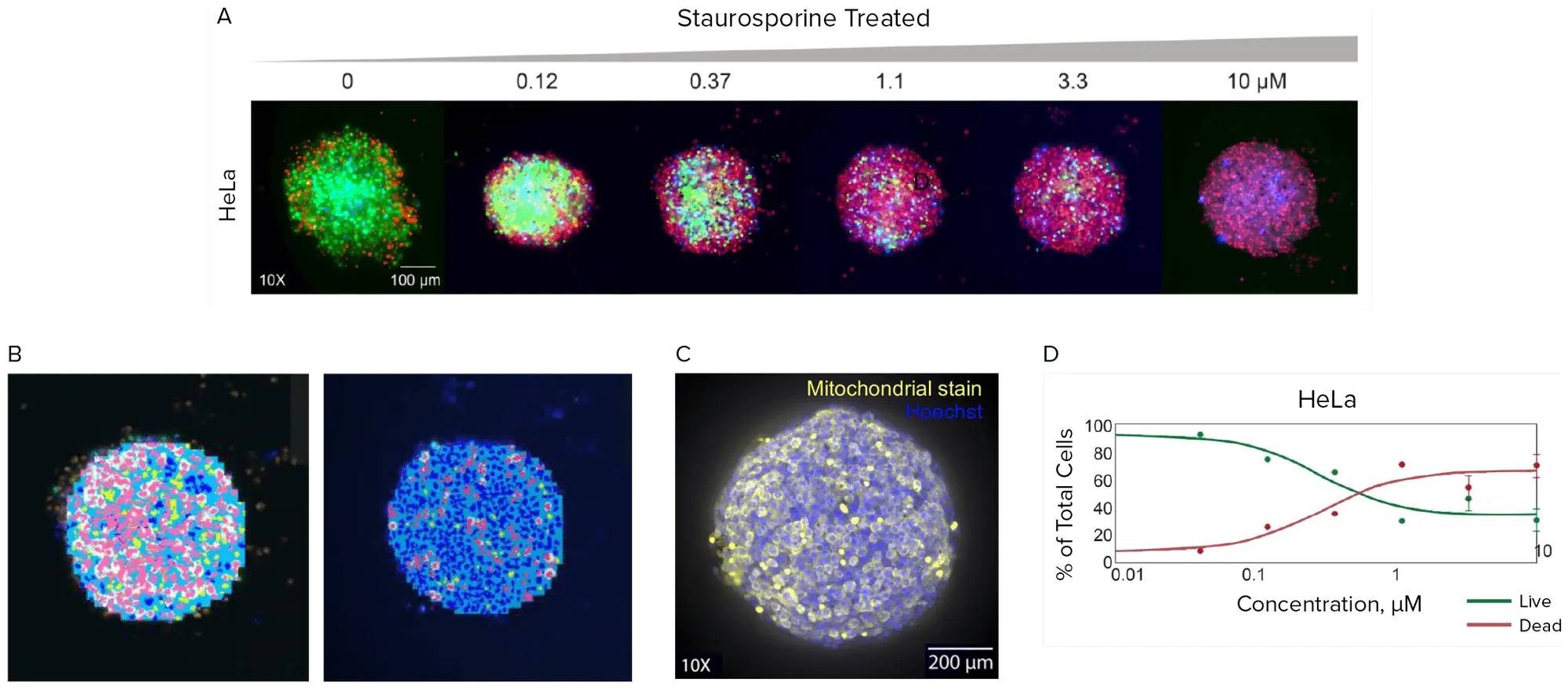
図3. 薬剤処理と染色です。A) スタウロスポリン(0~10 μM)の濃度を増加させて処理したHeLaスフェロイドの共焦点イメージング画像で、核染色(Hoechst、青)、細胞生存率染色(Calcein AM、緑)、細胞死染色(EthD-1、赤)を示します。画像は10X Plan Fluor対物レンズで撮影しました。B) 処理群と未処理群のスフェロイド領域(水色)、生細胞(ピンク)、死細胞(濃青)を示す画像解析マスクです。C) flowchip内で染色およびイメージングされた未処理HeLaスフェロイド(Hoechstおよび細胞生存率のミトコンドリアマーカーMitotracker™ Orange)。D) スタウロスポリンの異なる濃度(0.01~10 μM)で処理した際の生細胞と死細胞の割合を示すグラフです。
In vitro薬剤感受性アッセイと一次腫瘍3Dモデルにおけるバイオマーカー検出
患者由来オルガノイド(PDO)は、一次トリプルネガティブ乳がん由来のTU-BcX-4IC細胞から形成され、以前の報告(4)の通り緊密な球状構造に成長しました。ここでは、オルガノイド形成のためにマイクロパターンプレートを使用して方法をさらに最適化しました。24ウェルAggreWell™ 400マイクロウェルプレートの1ウェルを使用することで、約1,200個の均一サイズのPDOを生成できました。オルガノイドを作成するため、TU-BcX-4IC細胞をマイクロウェルあたり2,000細胞の密度で播種し、プレートを2日間インキュベートしてコンパクトな3Dオルガノイドを形成しました。NanoShuttleを100 μLウェルに添加し、オルガノイドをNanoShuttleと3時間インキュベートした後、PDOを収穫してflowchipに移送しました。本研究で使用した薬剤はロミデプシンとトラメチニブです。3Dオルガノイドは異なる濃度の薬剤で48時間処理されました。その後、Pu·MA System 3D MAG内で自動薬剤処理と免疫蛍光染色を行いました。生細胞は、前述の通りCalcein AM、Hoechst、Ethidium Homodimer 1で染色され、ImageXpress Micro Confocalシステムでイメージングし、MetaXpressソフトウェアのLive/Dead解析モジュールで解析しました(図5Aおよび5B)。画像は共焦点Zスタックとして取得され、細胞生存率解析のために2D投影画像に圧縮されました。多パラメータリードアウトが生成され、濃度応答曲線が解析されました(図4A、4B)。
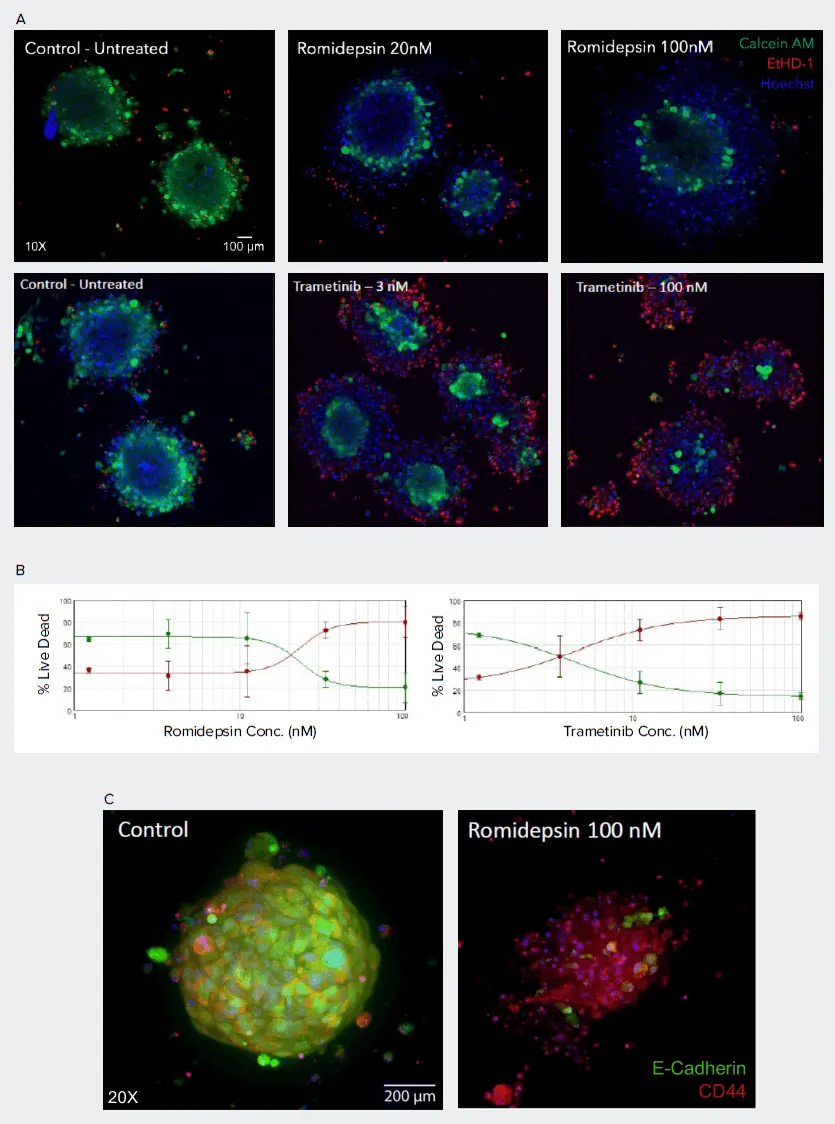
図4. PDOの薬剤処理アッセイです。A) ロミデプシン(上)およびトラメチニブ(下)で処理したPDOの共焦点画像で、核染色(Hoechst、青)、細胞生存率染色(Calcein AM、緑)、細胞死染色(EthD-1、赤)を示します。画像は10X対物レンズで取得した共焦点スタックの最大投影です。B) ロミデプシンおよびトラメチニブで処理したPDOの濃度応答曲線です。ロミデプシンおよびトラメチニブのEC₅₀値は、以前に2D細胞モデルで得られた結果と一致しました。C) E-cadherin(緑)およびCD44(赤)で標識されたPDOです。画像は20X水浸対物レンズで取得した共焦点スタックの最大投影です。ロミデプシン処理によりE-cadherinの消失とオルガノイドの破壊が確認されました。
生細胞と死細胞の割合は解析によって決定され、化合物の有効濃度の算出に使用されました。その後、サンプルは固定され、E-cadherinおよびCD44の特異的マーカーで再染色されました。
PDOの特異的マーカーに対する免疫蛍光染色は、ロミデプシン処理後にPu·MA System内で実施されました。E-cadherinおよびCD44マーカーは、図5Cに示すようにPDOで検出されました。共焦点画像はImageXpress Micro Confocalイメージングシステムで取得しました。結果は、薬剤処理によるPDOの破壊とE-cadherin発現の低下を示しました。
結論
私たちは、Pu·MA System 3D MAG上で磁性コーティングされた3D細胞マイクロティッシュを用いた改良されたアッセイワークフローを実証し、その後ImageXpress Micro Confocalシステムによるハイコンテントイメージングと解析を行いました。この統合ワークフローにより、以下の実施能力が向上します:オルガノイド/スフェロイドの自動処理、分泌因子のin situメディアサンプリング、薬剤処理と多パラメータ解析、バイオマーカーの免疫蛍光染色。
効率化されたワークフローとPu·MA Systemプロトコールを使用し、異なる薬剤と濃度に応答するさまざまな3D細胞モデルの染色とイメージングを示しました。自動薬剤処理、染色、サンプル処理、および生存率、マーカー発現、表現型変化のイメージング解析を実証し、3D腫瘍サンプルにおける薬剤感受性の迅速な評価に利用できることを示しました。
参考文献
- Human Organoids: Tools for Understanding Biology and Treating Diseases. Schutgens, F. and H. Clevers, (2020) 15(1): p. 211–234, Ann. Rev. of Pathology: Mech. of Disease.
- A brief history of organoids. Corro C. et al. (2020) 319: C151–C165, Am. J. Physiol.
- Three-dimensional tissue culture based on magnetic cell levitation. Souza, G.R. et a.l (2010) 5(4): 291, Nat. Nanotechnol.
- Drug resistance profiling if a new triple negative breast cancer patient-derived xenograft model. Matossian, M.D. et al (2019) 19(1): 205, BMC Cancer.
- High-Content Assays for Characterizing the Viability and Morphology of 3D Cancer Spheroid Cultures. Sirenko, O. et al. (2015) 13, 402, Assay and Drug Dev Tech.
謝辞
Matthew Burow博士およびMargarite Matossian博士(Tulane University)。NanoShuttleはGreiner Bio-Oneの好意によりご提供。
PDF版(英語)