Application Note モレキュラーデバイス マイクロプレートリーダーでの
MycoAlertマイコプラズマ検出アッセイ
- マイコプラズマ汚染の高感度かつ信頼性の高い検出
- 迅速な結果が得られるシンプルなアド・アンド・リード方式
- 結果の解釈が容易
PDF版(英語)
はじめに
マイコプラズマは、最も小さく最も単純な原核生物であり、細胞培養における一般的な汚染源です。マイコプラズマ汚染の兆候には、増殖速度の低下や遺伝子発現を含む細胞応答の変化などがあります。マイコプラズマは顕微鏡で細胞培養を観察するだけでは検出できないため、汚染の有無を判断するには高感度かつ信頼性の高いアッセイが必要です。従来のマイコプラズマ検出法は、時間のかかる染色やPCRプロトコールを必要とし、結果の解釈が難しい場合があります。
Lonza社の MycoAlert™ アッセイ および MycoAlert PLUS アッセイ は、発光マイクロプレートリーダーを使用して、細胞培養中の生存マイコプラズマを迅速かつ簡便に検出する方法を提供します。これらのアッセイは、主要なマイコプラズマ種に存在するマイコプラズマ特異的酵素を利用して汚染をスクリーニングします。MycoAlert PLUS アッセイ は次世代のキットで、標準のMycoAlertキットよりも高い発光強度を提供し、より広範な発光プレートリーダーでの使用や、未使用の培地、培地添加剤、水の検査にも対応可能です。両キットのセットアップ手順は同一です。
アッセイの第1ステップでは、MycoAlert試薬 を細胞培養上清に添加し、生存マイコプラズマを溶解して、背景ATPから光を生成する生物発光ルシフェラーゼ反応を開始します(図1)。第2ステップでは、MycoAlert基質 を添加し、放出されたマイコプラズマ酵素と反応してADPを追加のATPに変換します。その後、プレートリーダーで生物発光を検出し、MycoAlert基質添加前後のATP量を測定します。
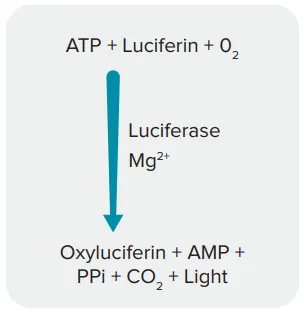
図1:ATP検出のための生物発光反応
基質添加の前後に発光プレートリーダーで測定を行い、その比率を算出することでマイコプラズマの存在を判定します。マイコプラズマ酵素が存在しない場合、2回目の測定値は1回目と比べて増加せず(MycoAlertアッセイでは比率 < 0.9、MycoAlert PLUSでは < 1.0)、マイコプラズマが陽性の場合は2回目の測定値が1回目より高くなります(比率 > 1.2)。
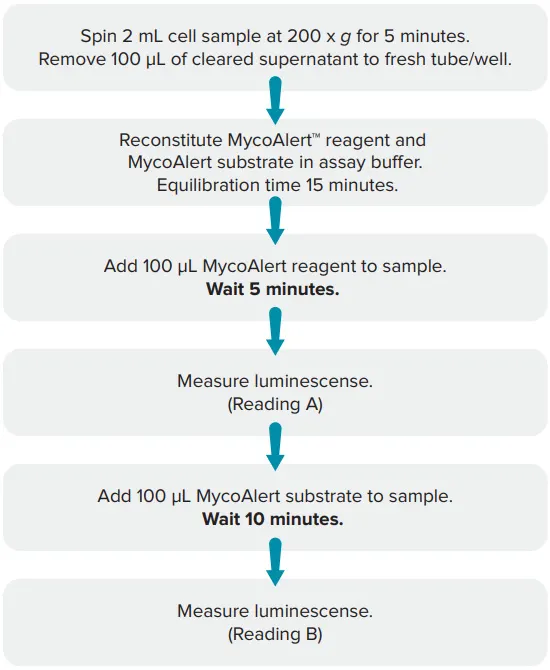
図2:MycoAlertアッセイのワークフロー ルミネッセンス測定値「Reading B」を「Reading A」で割ることで、マイコプラズマの存在(比率 > 1.2)または非存在(MycoAlertアッセイでは < 0.9、MycoAlert PLUSでは < 1.0)を示す比率を得ます。
このアプリケーションノートでは、モレキュラーデバイス製マイクロプレートリーダーのルミネッセンス検出モードが、MycoAlertアッセイを用いたマイコプラズマの信頼性の高い検出において、優れた感度と使いやすさを提供することを示します。オリジナルのMycoAlertアッセイキットと、感度が向上した新バージョンのMycoAlert PLUSの両方をテストし、モレキュラーデバイス製マイクロプレートリーダーとの互換性が確認されました。
材料
- MycoAlert Mycoplasma 検出キット(Lonza cat.)
- MycoAlert PLUS Mycoplasma Detection Kit(Lonza cat.)
- MycoAlert コントロールセット(Lonza cat.)
- 96ウェルポリスチレン白色ソリッドプレート(Greiner cat.)
- マイクロプレートリーダー
SpectraMax ® i3 マルチモードマイクロプレートリーダー
SpectraMax i3x マルチモードマイクロプレートリーダー
SpectraMax Paradigm® マルチモードマイクロプレートリーダー
SpectraMax M5マルチモードマイクロプレートリーダー
FilterMax™ F5 マルチモードマイクロプレートリーダー
SpectraMax Lマイクロプレートプレートリーダー
メソッド
MycoAlertおよびMycoAlert PLUSアッセイの手法は基本的に同じで、異なるのは使用するアッセイコントロールの濃度範囲のみです。各キットは、試薬を再構成した当日に使用しました。
各アッセイフォーマットに対して、MycoAlert陽性アッセイコントロールの濃度系列を表1に示す通りに調製しました。希釈はMycoAlertアッセイバッファーで行い、各サンプル100 µLを白色の平底96ウェルプレートに分注しました。サンプルは3つのレプリケートで実施しました。各ウェルにMycoAlert試薬を添加し、室温で5分間インキュベートしました。その後、モレキュラーデバイス製マイクロプレートリーダーの発光検出モードでプレートを測定しました(Read A)。次にMycoAlert基質をウェルに添加し、室温で10分間インキュベートした後、再度プレートを測定しました(Read B)。各サンプルの比率は「Read B ÷ Read A」で算出しました。両方の測定は、表2に示す機器設定で実施しました。データはSoftMax® Proソフトウェアで生成・解析され、最終結果はSoftMax Pro 6.5以降のバーグラフ機能を使用して表示されました。
| マイコアラート | マイコアラートプラス |
|---|---|
| 陽性コントロール | 陽性コントロール |
| 1:2 | 1:10 |
| 1:4 | 1:100 |
| 1:8 | 1:1000 |
| 1:16 | 1:10000 |
| 陰性コントロール | 陰性コントロール |
表1. MycoAlertおよびMycoAlert PLUSアッセイの標準希釈系列の調製 MycoAlert陽性アッセイコントロールは、指定された比率でMycoAlertアッセイバッファーに希釈されました。
| パラメータ | 設定 |
|---|---|
| 読み取りモード | 発光*(全波長) |
| 積分時間 | 1秒 |
| プレーティングタイプ | 96ウェルグライナー |
表2. MycoAlertアッセイの一般的な装置設定 SpectraMax Paradigmプレートリーダーは、本アッセイのシグナル検出に「発光検出カートリッジ」を使用します。他のすべてのテスト済みプレートリーダーは、統合された発光検出モードを使用します。
結果
各キットに対する発光リーダーの感度基準は、Lonza社によって定義されています。MycoAlertキットでは、アッセイコントロールサンプルは少なくとも1:8の希釈で比率 > 1.2を示す必要があります。MycoAlert PLUSキットでは、少なくとも1:1000の希釈で比率 > 1.2を示す必要があります。
モレキュラーデバイス製のすべてのマイクロプレートリーダー(発光検出モード搭載)は、MycoAlertおよびMycoAlert PLUSキットに対して、Lonza社が定める感度要件を上回る性能を示しました。図3には、SpectraMax i3x マルチモードマイクロプレートリーダーによるMycoAlertおよびMycoAlert PLUSアッセイの代表的なデータが示されています。表3には、各アッセイにおける最小必要希釈で得られた比率を、テストされたすべてのモレキュラーデバイス製プレートリーダーについてまとめています。
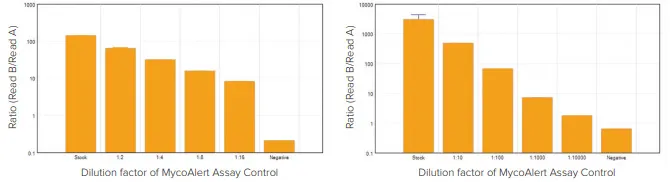
図3:SpectraMax i3xプレートリーダーによるMycoAlertアッセイコントロールの希釈系列検出感度 陰性サンプルにはMycoAlertアッセイバッファーのみが含まれています。各キットにおいて、リーダーは最も低い希釈濃度でも陽性として検出することができました。アスタリスクは、各キットで最小限検出可能であるべきアッセイコントロールの希釈濃度を示しています。左:MycoAlertアッセイキット/右:MycoAlert PLUSキット
| マイクロプレートリーダー |
マイコアラート比 (1:8アッセイコントロール) |
MycoAlert PLUS 比率
(1:1000アッセイコントロール) |
|---|---|---|
| SpectraMax i3x | 15.8 | 7.4 |
| SpectraMax M5 | 17.8 | 5.7 |
| SpectraMax Paradigm | 7.8 | 5.2 |
| FilterMax F5 | 9.8 | 2.9 |
| SpectraMax L | 9.8 | 9.0 |
表3:最小必要希釈におけるアッセイコントロールの比率 すべての比率は、必要とされる閾値1.2を上回りました。
結論
本資料で示された結果は、モレキュラーデバイス製のすべてのマイクロプレートリーダー(発光検出モード搭載)が、MycoAlertおよびMycoAlert PLUSアッセイによるマイコプラズマ検出において、Lonza社が定めた感度要件を上回る性能を有していることを確認するものです。両キットとも、マイコプラズマ汚染を示すわずかなアッセイシグナルの増加を容易に検出できます。
モレキュラーデバイス製マイクロプレートリーダーとMycoAlertアッセイを組み合わせることで、マイコプラズマの高感度かつ迅速な検出が可能となり、細胞培養の汚染を確実に検出し、監視作業における貴重な時間を節約できます。
PDF版(英語)