Application Note SpectraMax Plus 384マイクロプレートリーダーを使用したワイン中の残糖測定
- ワインサンプル中の分析物を直接定量
- 従来のシングルチューブ法に比べてスループットが向上
- SoftMax Proソフトウェアによる結果の自動計算
PDF版(英語)
はじめに
リンゴ酸、残糖、揮発性酸度、アンモニアの分析は、ワイン生産中の品質管理において非常に重要です。マイクロプレートフォーマットで実施される酵素アッセイは定量的であり、時間と労力の点でハイスループットを達成するのに役立ちます。残糖アッセイでは、分析物が酵素的に変換され、副産物としてNADPHが得られます。340nmの吸光度を測定してNADPH生成を測定することで、ワインサンプル中の分析物を直接定量することができます。ここでは、モレキュラーデバイス SpectraMax® Plus 384マイクロプレートリーダーとSoftMax® Proソフトウェアを使用して、ワイン中の残糖の酵素測定のデータを効率的に収集および解析する方法についてご説明します。
SpectraMax Plus 384マイクロプレートリーダーのユニークな機能の一部を紹介します:
- 波長範囲: 190-1000 nm、1 nm刻み、フィルター不要。
- 測定速度:96ウェル:9秒
- 384ウェル:29秒
- 温度 周囲温度より4℃高い温度から45℃まで
- キュベットポート: 標準キュベットおよび12 x 75 mm試験管を収納可能
- OD範囲 0-4 OD
ワイン中の残糖(RS)の酵素測定
酵素反応
(1) グルコース + ATP
![]()
グルコース-6-リン酸+ADP
(2)フルクトース+ATP
![]()
フルクトース-6-リン酸+ADP
(3)フルクトース-6-リン酸
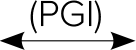
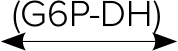
グルコース酸-6-リン酸 + NADPH + H+
HK:ヘキソキナーゼ
PGI ホスホグルコースイソメラーゼ
G6P-DH:グルコース-6-リン酸
デヒドロゲナーゼ
反応ダイナミクス
このアッセイは、ワイン中の2つの主要な糖、グルコースとフルクトースを測定します。NADPHの生成はグルコース-6-リン酸の酸化と化学量論的に関連していますので、グルコース+フルクトースの測定は340 nmにおけるNADPHの吸光度によって決定することができます。
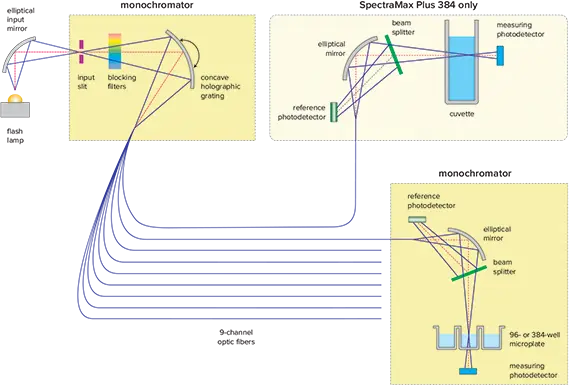
図1. SpectraMax Plus 384 optics
PathCheck センサー
PathCheck®センサーは、マイクロプレートウェル内のサンプルの光路長を測定する、モレキュラーデバイスの温度に依存しない機能です。マイクロプレートウェルの吸光度を1cmキュベットの吸光度に正規化する画期的な方法です。
ランベルト・ベールの法則では、吸光度 = E * C * Lとなります。
ここで
E = 吸光度(消衰係数)
C = 濃度
L = 光路長
キュベットの場合、光路は水平なので、光路長は固定され、1cm に等しいです。しかしマイクロプレートの場合、光路は垂直です。したがって、図2に示しますように、光路長は試料の体積に依存します。

図2. キュベットとマイクロプレートでは経路長が異なります
SoftMax Proソフトウェア
このソフトウェアは、機器の制御、データの収集、完全なデータ解析を行います。適切な機器設定と計算を含むカスタムプロトコルを事前に作成し、保存することができます。エンドユーザーは、設定済みのプロトコルを開くだけで、プロトコルのセットアップに時間をかけることなく、完全な結果と解析を得ることができます。

図3. ワイン中の残糖(RS)の測定。
材料
- SpectraMax Plus 384 マイクロプレートリーダー(モレキュラーデバイス)
- UV透過96ウェルマイクロプレート(Corning)
- トランスファーペットマイクロピペット(Drummond Scientific)
- マイクロピペット用マイクロチップ (Eppendorf)
- マイクロフュージチューブ用遠心機(Eppendorf)
- 容量1.5mLのマイクロフュージチューブ(Eppendorf)
- D-フルクトース(Fisher Scientific)
- ヘキソキナーゼ/グルコース-6-リン酸デヒドロゲナーゼ 30 mg(10 mL、Roche)
- ホスホグルコースイソメラーゼ 10 mg/mL (Roche)
- ポリビニルピロリドン (Fisher Scientific)
- TRIS (アムレスコ)
- MgSO4 - 7H2O (Fisher Scientific)
- ATP(Boehringer Mannheim)
- NADP(Boehringer Mannheim)
- 1.0M塩酸(Fisher Scientific)
フルクトース標準物質の調製
試薬を溶解するまで撹拌しました。決定係数(R)=1.000 の標準曲線が得られる標準品は、1.5 mL の凍結チューブに入れ、-4℃で保存しました。試薬が古すぎると理想的な標準曲線が得られない場合があります。
| Concentration | 0.1 g/100 mL | 0.2 g/100 mL | 0.4 g/100 mL |
|---|---|---|---|
|
DI H2O |
95 mL | 95 mL | 95 mL |
|
D-Fructose |
0.1 g | 0.2 g | 0.4 g |
|
Bring Volume To |
100 mL | 100 mL | 100 mL |
表1. フルクトース標準物質の調製
RS緩衝液の調製
ポリビニルピロリドン(PVP)2.0 g、TRIS 3.0 gおよびMgSO4 - 7H2O 0.5 gを400 mLビーカー中の350 mLの脱イオン(DI)H2Oに加えました。この溶液のpHを1.0 M HCl(≈36 mL)で7.6に調整しました。さらに、この溶液にATP 0.15 gとNADP 0.175 gを加え、メスフラスコで500 mLに調整しました。緩衝液は4℃で保存しました。
RS測定用ワインサンプルの処理
必要に応じて、表2に従ってワインサンプルを純水で希釈しました。濁ったサンプルは、希釈前または希釈後、分析前に遠心分離またはフィルタリングしました。純水1:10で希釈したサンプルには、1:10で希釈した4.0 g/100 mLの標準物質を添加しました。純水1:100で希釈した試料には、1:100で希釈した10.0 g/100 mLの標準液を添付しました。
| アッセイリミット | 希釈 | サンプル量 |
|---|---|---|
| 0.01~0.4 g/100 mL | 希釈不要 | 5 µL |
| 0.4-1.0 g/100 mL | 希釈不要 | 5 µL |
| 1.0-4.0 g/100 mL | 1:10 希釈 | 5 µL |
| 4.0-40.0 g/100 mL | 1:100 希釈 | 5 µL |
表2. RS測定用ワインサンプルの処理
方法
ステップ1:ブランク、標準品、サンプルを二重測定しました。
| 試薬ブランク | バッファー 300 µL | 純水 5 µL |
|---|---|---|
| スタンダード | バッファー 300 µL | スタンダード 5 µL |
| サンプル | バッファー 300 µL | サンプル 5 µL |
ステップ2:D-フルクトース標準物質を冷凍庫から取り出し、室温まで温めました。
ステップ3:標準品とサンプルの分析に必要な量の緩衝液を専用の「RS」ビーカーに計り取り、室温に温めました。このステップは、理想的な決定係数を得るために必要です。
ステップ4:ホスホグルコースイソメラーゼ(PGI)酵素を、表3の値に従って緩衝液に添加しました。PGIは、酵素を変性させないように穏やかに、しかし十分にバッファーに混合しました。
| 必要バッファー量 | PGI添加量 |
|---|---|
| 10 µL | 14 µL |
| 50 µL | 28 µL |
| 100 µL | 56 µL |
| 150 µL | 84 µL |
| 200 µL | 112 µL |
表3. 反応バッファー量あたりのホスホグルコースイソメラーゼ必要量の計算。
ステップ5:300μLのマルチチャンネルピペットを用いて、各ウェルに300μLのバッファーを分注しました。
ステップ6:5µLのDI H2O、標準品またはサンプルを適切なウェルに分注しました。
ステップ7:試薬を上下にピペッティングして混合しました(トリチュレーション)。
ステップ8:プレートを30秒間ボルテックスして混合し、吸光マイクロプレートリーダーで最初の吸光度を測定しました。
ステップ9:最初の読み取り値の直後に、1~20 µLのマルチチャンネルピペットを用いて各ウェルに5 µLのHK/G6P-DHを分注しました。
ステップ10: プレートを30秒間ボルテックスして混合し、室温で21分間インキュベートしました。
ステップ11:21分間のインキュベーション後、マイクロプレートリーダーの同じ機器設定で「Final」読み取りを行った。
機器のセットアップ
機器はSoftMax Proソフトウェアでプログラムしました。設定はソフトウェアのplate sectionで調整しました(図4)。表4にRSアッセイに使用した機器設定を示します。図4は波長設定と "PathCheck "選択のスクリーンショットです。
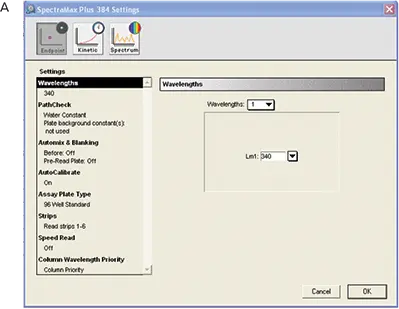
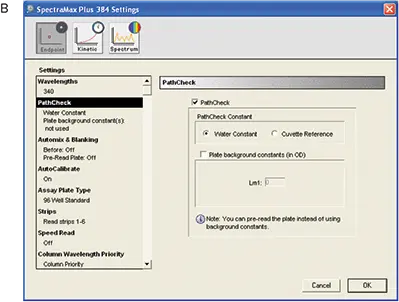
図4. RS アッセイ用の機器Setting。A:全体的なSetting、B:PathCheckセンサーのSetting
| Parameter | Setting |
|---|---|
| Read Type | Endpoint |
| Wavelength | 340 nm |
| PathCheck | PathCheck選択、Water Constant(no plate background constant) |
| Automix & Blanking | Off |
| AutoCalibrate | On |
| Assay Plate Type | 96-Well Standard |
| Strips | Selected as needed |
表 4. RSアッセイ 機器の設定
同じplate sectionを2つ作成しました。最初のplate sectionは、すべての試薬を含むが酵素を含まないプレートの読み取りを行いました。2番目のplate sectionは、酵素を用いた実際の反応です。最初のplate sectionから読み取った光学濃度は、還元設定により2番目のplate sectionの光学濃度から差し引かれました。
RSアッセイ用テンプレートのセットアップ
標準品とサンプルをマイクロプレートのウェルに配置するためのテンプレートがソフトウェアで設定されました。テンプレートのレイアウトはフレキシブルなので、サンプルやレプリカを簡単に追加することができます。最初のプレートにはテンプレートを設定しませんでした。最終プレートでは、標準品と未知検体が割り当てられました。各標準物質の濃度は、ウェルをクリックしてボックスに適切な濃度を入力することで割り当てました。範囲は0-0.4 g/100 mLでした(図5)。
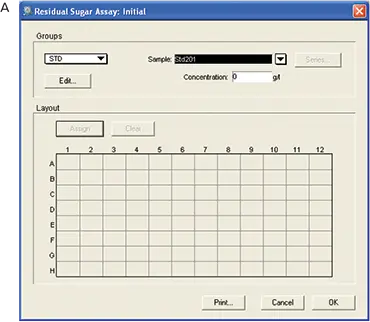
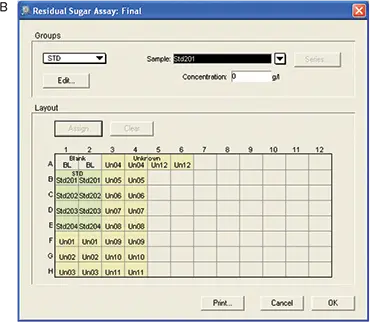
図5. RSアッセイ用テンプレートのセットアップ。A: 初期プレート-テンプレートはセットされていません。B: 最終プレート-プレート、標準品、未知検体を含むテンプレート。
Reductionのセットアップ
最終プレートでは、実際に酵素を反応させました。初期プレートの光学濃度測定値は、還元設定により最終プレートの光学濃度測定値から差し引かれました(図6)。したがって、プレートブランクは使用しなかったです。プレートブランクは品質管理のために実験に組み込まれました。
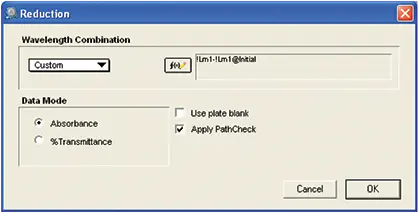
図6. データのReduction。最終プレートの同じウェルの光学濃度から初期プレートの各ウェルの光学濃度を差し引くために使用されるカスタム式を示す縮小セットアップします。計算にはPathCheckセンサーの値が適用されました。
結果
実験は「材料と方法」のセクションに記載されているように実施しました。酵素を除く反応混合物の全成分を封じ込めたプレートで、ベースラインの読み取りを行いました(図7、パネルA)。反応混合物に酵素を添加した後、プレートを室温で 21 分間インキュベートし、最終的な読み取りを行いました(図 7、パネル B)。
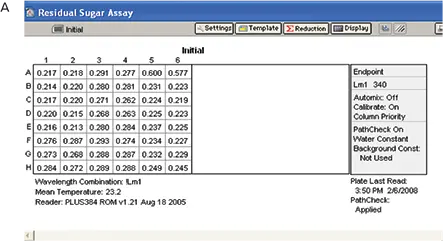
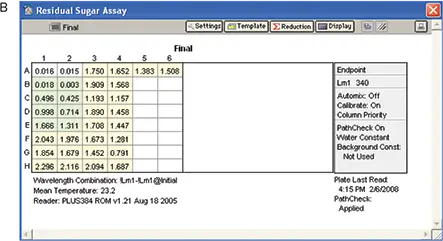
図7. RSアッセイの結果。A: すべての試薬を添加し、酵素を添加しなかったプレーティング。B:酵素を添加し、インキュベートした後のプレーティング。
SoftMax Proソフトウェアは、標準物質の平均、標準偏差、%CVを自動的に計算し、結果をグループセクションに表示しました(図8)。
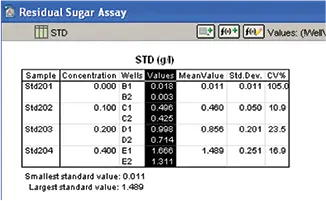
図8. 標準の計算。平均、標準偏差、%CV の計算を伴うグループセクション標準です。
標準曲線
グループセクション "STD "の情報を用いて、X軸に濃度、Y軸に反復試料の平均OD値をとり、標準曲線を作成しました(図9)。標準偏差はエラーバーとして使用され、linear curve fit 処理がプロットに割り当てられました。この標準曲線は、"Unknown "と表示されたワインサンプルの残糖濃度の測定に使用されました。
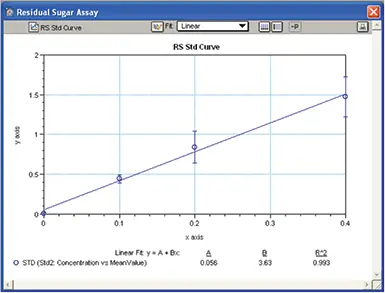
図9. RSアッセイ standard curve。標準曲線をプロットし、ワインサンプル中の残糖濃度の算出に使用しました。
"Unknown"と指定されたグループセクションには、テンプレートで「Unknown」と指定されたサンプルからのデータが自動的に入力されました。
各サンプルの残留糖分は、 standard curveを用いてソフトウェアで計算されました(図10および11)。
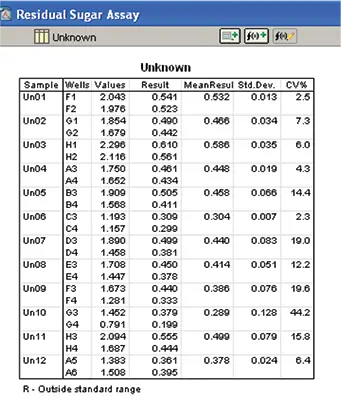
図10. ワインサンプル中の残糖濃度の算出。標準曲線を用いてワインサンプル中の残糖濃度を算出しました。
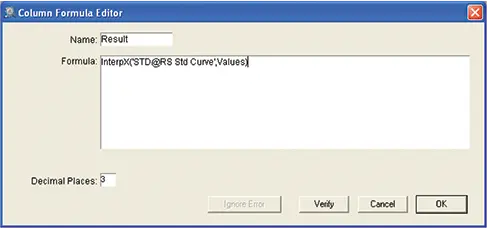
図11. standard curveを補間するためのCustom formula。standard curveから内挿法でワインサンプルの残留糖分を自動計算した "Result” 列の計算式です。
結論
SpectraMax Plus 384マイクロプレートリーダーは、ワイン中の残糖(RS)およびリンゴ酸(ML)の酵素的定量測定に最適です。
以下のような利点があります:
- ワインサンプル中の分析物を直接定量
- 従来のシングルチューブ法に比べてスループットが向上
- SoftMax Proソフトウェアによる結果の自動計算
- コスト効率と時間効率が高いです。
- SpectraMax Plus 384リーダーのチューナビリティとPectraCheck®センサー機能は、より高い精度と正確性を達成するのに役立ちます。
- SoftMax Proソフトウェアは、複雑で大規模なデータセットの解析や計算に便利なツールです。あらかじめ書き込まれたすぐに使用できるプロトコル、カスタムプロトコル、適切なグラフオプションを提供します。
- 吸光度検出モードを備えた他のモレキュラーデバイス プレートリーダー(SpectraMax i3x マルチモードマイクロプレートリーダーなど)も、このアプリケーションに使用できます。
- スループットの向上が必要な場合は、モレキュラーデバイス StakMax®マイクロプレート処理システムをSpectraMaxマイクロプレートリーダーと統合することで、20、40、50マイクロプレートのバッチ処理を自動化できます。
PDF版(英語)